
【题目】现有一包由3.2g铜、13g锌和2g 碳组成的粉末,放到一定量的AgNO3溶液中,完全反应后得到的固体为m种,溶液中溶质为n种.下列说法中不正确的是( )
A. 若m=2,则n=2或3 B. 若固体中金属的质量为 48g,则m=4
C. 当m=3时,溶液可能呈蓝色 D. 反应后固体的质量不可能超过56g
【答案】B
【解析】由金属活动性顺序表可知,金属的活动性Zn>Cu>Ag,由3.2g铜、13g锌和2g 碳组成的粉末,放到一定量的AgNO3溶液中,Zn首先与硝酸银溶液反应,Zn反应完成时,Cu再与硝酸银反应.碳与硝酸银不反应.化学方程式为:①Zn+2AgNO3=2Ag+Zn(NO3)2;②Cu+2AgNO3=2Ag+Cu(NO3)2A、当m=2时,则得到的固体为银和碳,Cu和Zn全部反应,硝酸银溶液足量.恰好反应时,溶液中的溶质为硝酸铜和硝酸锌;硝酸银过量时,溶液中的溶质为硝酸铜、硝酸锌和硝酸银,因此,n=2或3,故A正确;B、当上述两个反应分别恰好进行完全时,设生成银的质量分别为x,y
Zn+2AgNO3=2Ag+Zn(NO3)2
65 216
13g x
![]() 解得:x=43.2g
解得:x=43.2g
Cu+2AgNO3=2Ag+Cu(NO3)2
64 216
3.2g y
![]() 解得:y=10.8g
解得:y=10.8g
当锌完全反应时,金属的质量为:3.2g+43.2g=46.4g,铜完全反应时,金属的质量最大是:43.2g+10.8g=54g,由于金属的质量是48g,46.4g<48g<54g.由此可知,锌完全反应,部分铜已参加反应,所以,固体物质有银、铜和碳三种,即m=3,故B不正确;C、由上述计算分析可知,当m=3时,溶液可能呈蓝色,故C正确;D、由上述计算分析可知,反应后固体的质量不可能超过54g+2g=56g,故D正确.故选B.


科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 葡萄糖、果糖和蔗糖都能发生水解
B. 糖类、油脂、蛋白质都只是由C、H、O 三种元素组成的
C. 糖类、油脂、蛋白质都是高分子化合物
D. 油脂有油和脂肪之分,但都属于酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖啡酸(下式中的A)是某种抗氧化剂成分之一,A与FeCl3溶液反应显紫色. 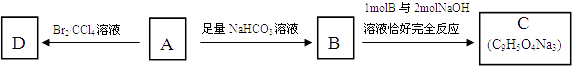
(1)咖啡酸中含氧官能团的名称为 .
(2)咖啡酸可以发生的反应是(填写序号).①氧化反应 ②加成反应 ③酯化反应 ④加聚反应 ⑤消去反应
(3)咖啡酸可看作1,3,4﹣三取代苯,其中两个相同的官能团位于邻位,取代基中不含支链.则咖啡酸的结构简式为 .
(4)3.6g咖啡酸与足量碳酸氢钠反应生成气体(标准状况)mL.
(5)蜂胶的主要活性成分为CPAE,分子式为C17H16O4 , 该物质在一定条件下可水解生成咖啡酸和一种醇,该醇为芳香醇,且分子结构中无甲基,则咖啡酸跟该芳香醇在一定条件下反应生成CPAE的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】12.0g某液态有机化合物A完全燃烧后,生成14.4gH2O和26.4g CO2 . 测得有机化合物A的蒸气与H2的相对密度是30,求: 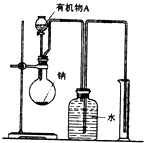
(1)有机物A的分子式 .
(2)用如图所示装置测定有机物A的分子结构,实验数据如下(实验数据均已换算为标准状况):a mL(密度为ρg/cm3)的有机物A与足量钠完全反应后,量筒液面读数为bmL,若1mol A分子中有x mol氢原子能跟金属钠反应,则x的计算式为(可以不化简).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析下表中各项的排布规律,按此规律排布第26项应为( )
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
C2H4 | C2H6 | C2H6O | C2H6O2 | C3H6 | C3H8 | C3H8O | C3H8O2 | C4H8 | C4H10 |
A.C7H16
B.C7H14O2
C.C8H18
D.C8H18O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO是火力发电厂释放出的主要尾气,为减少对环境污染,发电厂试图采用CO与Cl2在催化剂的作用下合成光气(COCl2).某温度下,向2L的密闭容器中投入一定量的CO和Cl2 , 在催化剂的作用下发生反应:CO(g)+Cl2(g)COCl2(g)△H=a kJ/mol
反应过程中测定的部分数据如下表:
t/min | n (CO)/mol | n (Cl2)/mol |
0 | 1.20 | 0.60 |
1 | 0.90 | |
2 | 0.80 | |
4 | 0.20 |
(1)反应0~2min末的平均速率v(COCl2)=mol/(Lmin).
(2)在2min~4min间,v(Cl2)正v(Cl2)逆 (填“>”、“=”或“<”),该温度下K= .
(3)在图1中画出0~4min末n(COCl2)随时间的变化示意图 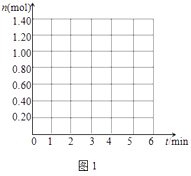
(4)已知X、L可分别代表温度或压强,如图2表示L一定时,CO的转化率随X的变化关系.X代表的物理量是;a0 (填“>”,“=”,“<”),依据是 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中存在较多的H+、SO42-、NO3-,则该溶液中还可能大量存在的离子组是
A. Mg2+、NH4+、Cl- B. Mg2+、Ba2+、Br-
C. Na+、Cl-、I- D. Al3+、HCO3-、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com