
| A. | 二氧化硅和氯化镁熔化 | B. | 碘和氯化铵受热变成气体 | ||
| C. | 碘和干冰的升华 | D. | 氯化钠和氯化氢溶于水 | ||
| E. | 硅和蔗糖的熔化 | F. | 酒精和水的挥发 |
分析 原子晶体中需要克服共价键,分子晶体中需要克服分子间作用力,离子晶体中需要克服离子键,金属晶体需要克服金属键,根据晶体类型判断即可,据此分析解答.
解答 解:A.二氧化硅属于原子晶体,需要克服共价键,氯化镁属于离子晶体,需要克服离子键,所以克服作用力不同,故A不选;
B.碘属于分子晶体,需要克服分子间作用力,氯化铵属于离子晶体,需要克服离子键,所以克服作用力不同,故B不选;
C.碘和干冰都属于分子晶体,需要克服分子间作用力,故C选;
D.氯化钠属于离子晶体,需要克服离子键,氯化氢属于分子晶体,需要克服共价键,所以克服作用力不同,故D不选;
E.硅属于原子晶体,需要克服共价键,蔗糖属于分子晶体,需要克服分子间作用力,所以克服作用力不同,故E不选;
F.酒精和水都属于分子晶体,需要克服分子间作用力,所以克服作用力相同,故F选;
故选CF.
点评 本题考查了晶体的类型,明确晶体的构成微粒是解本题关键,难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

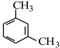 ;
;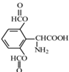 、
、 ;
; +CH3CH=CH2$\stackrel{AlCl_{3}}{→}$
+CH3CH=CH2$\stackrel{AlCl_{3}}{→}$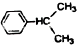 结合相关信息,请写出以
结合相关信息,请写出以 、CH2=CH2和
、CH2=CH2和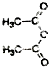 为原料制备
为原料制备 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在Cu2O、Cu2S中Cu元素化合价都是+1价 | |
| B. | 反应中Cu元素被氧化,S元素被还原 | |
| C. | Cu2S在反应中既是氧化剂,又是还原剂 | |
| D. | 每生成6.4g Cu,反应中转移0.1 mole- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
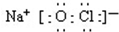 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.24g | B. | 3.36g | C. | 5.60g | D. | 10.08g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
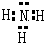 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2是硅酸的酸酐,但不能由SiO2直接制硅酸 | |
| B. | 二氧化硅是通讯材料光导纤维的主要原料 | |
| C. | 氧化铝陶瓷、碳化硅陶瓷都是重要的高温结构陶瓷 | |
| D. | 二氧化硅熔点与干冰相差不大,它们都是酸性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com