
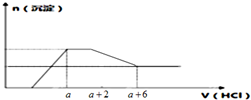
 某溶液中可能含有OH-、CO32-、AlO2-、SiO32-、SO42-、Na+、Fe3+、Mg2+、Al3+等离子.当向该溶液中加入一定物质的量浓度的盐酸时,发现生成沉淀物质的量随盐酸的体积变化的如图所示,下列说法正确的是( )
某溶液中可能含有OH-、CO32-、AlO2-、SiO32-、SO42-、Na+、Fe3+、Mg2+、Al3+等离子.当向该溶液中加入一定物质的量浓度的盐酸时,发现生成沉淀物质的量随盐酸的体积变化的如图所示,下列说法正确的是( )| A、原溶液一定含有Na2SO4 |
| B、反应最后形成的溶液中的溶质为NaCl |
| C、原溶液中一定含有的阴离子是OH-、CO32-、AlO2-、SO42- |
| D、原溶液中含有CO32- 与AlO2-的物质的量之比为3:4 |


科目:高中化学 来源: 题型:
| A、蒸发:利用物质颗粒的大小 |
| B、萃取:利用物质的溶解度不同 |
| C、过滤:利用物质的沸点不同 |
| D、蒸馏:利用物质的沸点不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、热的纯碱去污效果更好 |
| B、在H2、I2和HI组成的平衡体系加压后,混合气体颜色变深 |
| C、实验室可用排饱和食盐水的方法收集氯气 |
| D、高压下有利于提高合成氨的产率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
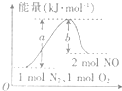
| A、该反应为放热反应 | ||
| B、该反应每生成2 mol NO,吸收b kJ热量 | ||
| C、该反应中反应物的总能量高于生成物的总能量 | ||
D、该反应吸收
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、镁原子:1s22s22p63s2 |
| B、铝离子:1s22s22p6 |
| C、S2-:1s22s22p63s23p4 |
| D、氟原子:1s22s22p5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、光化学烟雾是氮氧化物受紫外线照射后产生的O3直接与空气中的一些碳氢化合物作用后生成的一种有毒烟雾 |
| B、石油液化气、汽油和石蜡的主要成分都是碳氢化合物 |
| C、绿色化学的核心是应用化学原理对环境污染进行治理 |
| D、CCl4曾用作灭火剂,但因与水在高温下反应会产生有毒物质,现已被禁用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.0×10-7 mol?L-1 |
| B、1.0×10-6 mol?L-1 |
| C、1.0×10-2 mol?L-1 |
| D、1.0×10-12 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com