
| c3(CO2) |
| c3(CO) |
| c3(CO2) |
| c3(CO) |
| c3(CO2) |
| c3(CO) |
| c3(CO2) |
| c3(CO) |
| ||
| 10min |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解
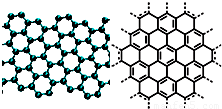
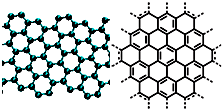 A.美国《科学》杂志评出的2009年十大科学突破之一是石墨烯的研究和应用方面的突破.石墨烯具有原子级的厚度、优异的电学性能、出色的化学稳定性和热力学稳定性.制备石墨烯方法有石墨剥离法、化学气相沉积法等.石墨烯的球棍模型及分子结构示意图如右:
A.美国《科学》杂志评出的2009年十大科学突破之一是石墨烯的研究和应用方面的突破.石墨烯具有原子级的厚度、优异的电学性能、出色的化学稳定性和热力学稳定性.制备石墨烯方法有石墨剥离法、化学气相沉积法等.石墨烯的球棍模型及分子结构示意图如右: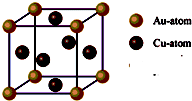
查看答案和解析>>
科目:高中化学 来源: 题型:



| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2011年高考化学总复习30分钟限时训练:专题16 铁铜及其化合物 题型:022
有七种金属:钠、铝、铁、锡、铜、银、金,它们的标号分别为A、B、C、D、E、F、G.
①常温下,只有A和水反应生成氢气;
②D、E、G都能和稀硫酸反应生成氢气;
③D、E、G中只有D与NaOH溶液反应;
④B、F组成原电池时,F为正极;
⑤将G、E组成的合金暴露在潮湿的空气中,经一段时间后,合金的表面有G的化合物出现;
⑥用石墨电极电解含有相同物质的量浓度的B和C两种金属的硝酸盐溶液,B的单质先析出.回答下列问题:
(1)B的元素符号是________;G元素在元素周期表中的位置是________.
(2)D的最高价氧化物与A的最高价氧化物对应水化物发生反应的离子方程式为________.D的单质与G的最高价氧化物发生反应的化学方程式为________,该反应在生产中有重要应用,被称为________反应.
(3)写出⑥中的电极反应式:阳极:________,阴极________.
(4)将C的氯化物溶液蒸干灼烧得到的固体物质是________,原因是________(用必要的文字和离子方程式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源:2009-2010学年江苏省盐城市高三(上)期中化学试卷(解析版) 题型:解答题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com