
| A. | 除去镁粉中少量的铝粉,加足量氢氧化钠溶液反应后,过滤 | |
| B. | 做水的蒸馏实验时,要在烧瓶内加几粒沸石以防止暴沸 | |
| C. | 金属钠可以保存在煤油里 | |
| D. | 可用过滤的方法除去氢氧化铁胶体中的氯化铁溶液 |
分析 A.Al与NaOH溶液反应,而Mg不能;
B.水加热时易沸腾;
C.Na的密度比煤油的密度大,且与煤油不反应;
D.胶体与离子均可透过滤纸.
解答 解:A.Al与NaOH溶液反应,而Mg不能,则加足量氢氧化钠溶液反应后,过滤可除去铝粉,故A正确;
B.水加热时易沸腾,则蒸馏时要在烧瓶内加几粒沸石以防止暴沸,故B正确;
C.Na的密度比煤油的密度大,且与煤油不反应,可隔绝氧气与水,则金属钠可以保存在煤油里,故C正确;
D.胶体与离子均可透过滤纸,则过滤的方法不能除去氢氧化铁胶体中的氯化铁溶液,应选渗析法,故D错误;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、性质差异及混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:解答题
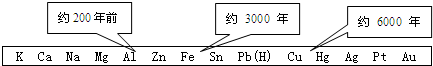
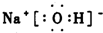 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ② | B. | ②③⑤ | C. | ②③ | D. | ①②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
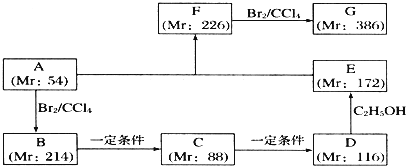
 )是一种香料,一种合成路线如下:
)是一种香料,一种合成路线如下: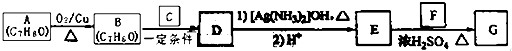 已知以下信息:
已知以下信息: ;
; +CH3CHO$\stackrel{一定条件}{→}$
+CH3CHO$\stackrel{一定条件}{→}$ +H2O.
+H2O. +(CH3)2CHCH2CH2OH$→_{△}^{浓硫酸}$
+(CH3)2CHCH2CH2OH$→_{△}^{浓硫酸}$ +H2O,反应类型为酯化反应.
+H2O,反应类型为酯化反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
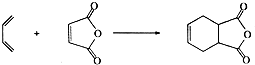
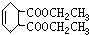 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 W、X、Y、Z、R是五种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10.X和Ne原子的核外电子数相差1.Y的最高价氧化物对应水化物是医用胃酸中和剂中的一种.R和W具有相同的最外层电子数.Z在同周期主族元素中原子半径最小.
W、X、Y、Z、R是五种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10.X和Ne原子的核外电子数相差1.Y的最高价氧化物对应水化物是医用胃酸中和剂中的一种.R和W具有相同的最外层电子数.Z在同周期主族元素中原子半径最小.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com