
【题目】在图所示物质的转化关系中,D在常温下为无色无味的液体(反应条件均已省略).请回答下列问题: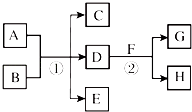
(1)高温下发生的反应②中,若F为常见的金属单质,H是非金属单质,用化学方程式表示G的一个重要用途: .
(2)若F为淡黄色粉末,①写出反应②的化学方程式并用双线桥标出电子转移的方向和数目 .
②F的电子式 .
(3)若A是一种强酸,B是一含有两种金属元素的盐,且其水溶液显碱性,写出①反应的离子方程式 .
(4)若A、F、H是短周期且相邻的两个族的元素单质,且反应均在溶液中进行,请写出:①的离子方程式;
②的化学方程式 .
【答案】
(1)Fe3O4+4CO ![]() 3Fe+4CO2
3Fe+4CO2
(2)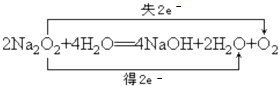 ;
;![]()
(3)AlO2﹣+4H+=Al3+2H2O
(4)Cl2+2OH﹣=Cl﹣+ClO﹣+H2O;2F2+2H2O=4HF+O2
【解析】解:(1)D常温常压下为无色无味液体,可判断D为水.高温下与水反应的常见金属单质可以是铁,同时放出无色气体H为H2 , G为Fe3O4 , Fe3O4的重要用途有炼铁、铝热反应等,反应方程式为:Fe3O4+4CO ![]() 3Fe+4CO2等,所以答案是:Fe3O4+4CO
3Fe+4CO2等,所以答案是:Fe3O4+4CO ![]() 3Fe+4CO2;(2)F为淡黄色粉末,且能与水反应生成非金属单质,则F是Na2O2 . ①用双线桥标出反应②的电子转移的方向和数目为:
3Fe+4CO2;(2)F为淡黄色粉末,且能与水反应生成非金属单质,则F是Na2O2 . ①用双线桥标出反应②的电子转移的方向和数目为: 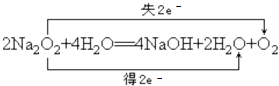 ,所以答案是:
,所以答案是: 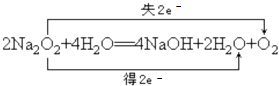 ;②Na2O2的电子式为
;②Na2O2的电子式为 ![]() ,所以答案是:
,所以答案是: ![]() ;(3)B是含有两种金属形成的盐,且溶液呈碱性,说明是弱酸盐,常见的B为偏铝酸盐,①反应的离子方程式为AlO2﹣+4H+=Al3+2H2O,所以答案是:AlO2﹣+4H+=Al3+2H2O;(4)单质A能与B反应生成三种物质,其中之一为水,其相邻元素与水反应生成非金属单质可判断,符合条件的反应只有Cl2和碱反应生成氯化物、次氯酸盐和水,H2O与F2反应可生成HF和O2 . 反应①的离子方程式为:Cl2+2OH﹣=Cl﹣+ClO﹣+H2O,反应②的化学方程式:2F2+2H2O=4HF+O2 , 所以答案是:Cl2+2OH﹣=Cl﹣+ClO﹣+H2O;2F2+2H2O=4HF+O2 .
;(3)B是含有两种金属形成的盐,且溶液呈碱性,说明是弱酸盐,常见的B为偏铝酸盐,①反应的离子方程式为AlO2﹣+4H+=Al3+2H2O,所以答案是:AlO2﹣+4H+=Al3+2H2O;(4)单质A能与B反应生成三种物质,其中之一为水,其相邻元素与水反应生成非金属单质可判断,符合条件的反应只有Cl2和碱反应生成氯化物、次氯酸盐和水,H2O与F2反应可生成HF和O2 . 反应①的离子方程式为:Cl2+2OH﹣=Cl﹣+ClO﹣+H2O,反应②的化学方程式:2F2+2H2O=4HF+O2 , 所以答案是:Cl2+2OH﹣=Cl﹣+ClO﹣+H2O;2F2+2H2O=4HF+O2 .


 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的是( )
A.常温下铝和浓硫酸、浓硝酸不反应
B.两份相同质量的铝粉,分别与足量的稀硫酸和氢氧化钠溶液反应,产生的氢气前者多
C.合金的熔点一般比组成它的各成分的熔点都高
D.工业上常利用铝热反应冶炼难熔的金属,如钒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下图装置中,加热试管内的白色固体A(A的焰色反应为黄色),生成白色固体B并放出气体C和D,这些气体通过甲瓶的浓硫酸后,C被吸收;D进入乙瓶跟另一淡黄色固体E反应生成白色固体B和气体F;丙瓶中的NaOH溶液用来吸收剩余的气体D。

(1)写出各物质的化学式:
A______; B_______; C________; D______; E_______; F___________。
(2)写出试管中及丙瓶中反应的化学方程式:_______________;__________________。
(3)等物质的量A、B分别与足量的盐酸反应生成气体的体积________(填“一样多”、“前者多”、“后者多”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,反应2SO2+O2 ![]() 2SO3 , 达到平衡时,n(SO2):n(O2):n(SO3)=2:3:4.缩小体积,反应再次达到平衡时,n(O2)=0.8mol,n(SO3)=1.4mol,此时SO2的物质的量应是( )
2SO3 , 达到平衡时,n(SO2):n(O2):n(SO3)=2:3:4.缩小体积,反应再次达到平衡时,n(O2)=0.8mol,n(SO3)=1.4mol,此时SO2的物质的量应是( )
A.0.6 mol
B.0.4 mol
C.0.8 mol
D.1.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种只含Al、Fe、Cu的合金,称取a g样品,设计下列实验流程分析该合金的组成 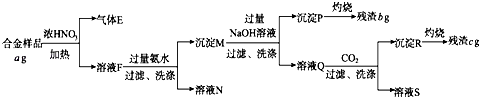
下列相关叙述正确的是( )
A.若向溶液F中加入K4[Fe(CN)6]溶液,产生蓝色沉淀,说明溶液F中含有Fe2+
B.溶液N为深蓝色,说明溶液N中含大量Cu2+
C.合金样品中Cu的质量分数为 ![]() ×100%
×100%
D.合金样品中Al的质量分数为 ![]() ×100%
×100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将0.2mol的碘化氢充入1L的密闭容器中,充分反应,达到平衡后,测得c(H2)=0.08mol/L.
(1)求该反应的平衡常数.
(2)在上述温度下,该容器中若充入碘化氢0.4mol,求达到平衡时碘化氢的转化率和氢气的物质的量浓度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.NH3是极性分子,分子中N原子是在3个H原子所组成的三角形的中心
B.CCl4是非极性分子,分子中C原子处在4个Cl原子所组成的正方形的中心
C.H2O是极性分子,分子中O原子不处在2个H原子所连成的直线的中央
D.CO2是非极性分子,分子中C原子不处在2个O原子所连成的直线的中央
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子的立体构型可用sp2杂化轨道来解释的是( )
①BF3 ②CH3═CH2 ③苯 ④CH≡CH ⑤NH3 ⑥CH4 ⑦HCHO.
A.①②③⑦
B.①⑤⑥
C.②③④⑦
D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液只含Cl![]() 、CO
、CO![]() 、SO
、SO![]() 、Na
、Na![]() 、K
、K![]() 、Mg
、Mg![]() 六种离子中的某几种。经实验:
六种离子中的某几种。经实验:
①原溶液![]() 白色沉淀;
白色沉淀;
②原溶液中加BaCl2溶液不产生沉淀;
③原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。回答下列问题:
(1)试分析原溶液中一定含有的离子是______________,一定不含有的离子是_______,可能含有的离子是______________。
(2)有的同学认为实验③可以省略,你认为是否正确(填“是”或“否”)_________,说明理由_________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com