
分析 (1)已知:Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g),△H1=-25KJ/mol…①,
3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g),△H2=-47KJ/mol…②,
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g),△H3=19KJ/mol…③,
根据盖斯定律将方程式变形$\frac{(3×①-②-2×③)}{6}$得:Fe(s)+CO(g)═Fe(s)+CO2(g),△H;
(2)①依据题意,反应物为Co2+与肼(N2H4)、碱性条件下存在OH-,生成物为:钴单质,据此得出Co的化合价降低,故N的化合价升高,只能为0价,即氮气,依据氧化还原反应得失电子守恒回答即可;
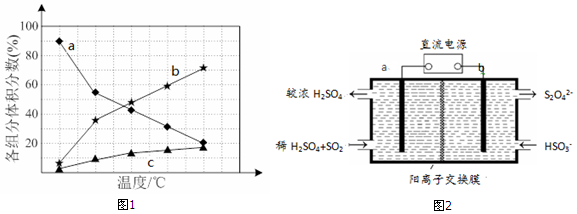
②根据化学平衡状态,反应的正逆反应速率相同,各成分含量保持不变分析;据图象分析;据影响平衡移动的因素判断;
(3)①依据图示可知,二氧化硫被氧化为硫酸根,所以二氧化硫所在的区为阳极区,阳极区发生反应SO2-2e-+2H2O═SO42-+4H+,阳极与电源的正极a相连,b为电源负极,阴极的电极反应式为:2HSO3-+2H++2e-═S2O42-+2H2O,阳离子交换膜只允许阳离子通过,电解时,阳离子移向阴极,据此分析;
②该装置吸收SO2的原理是SO2在 a极发生氧化反应,电极反应式:SO2-2e-+2H2O=4H++SO42-,H+通过阳离子交换膜进入b 极室.
解答 解:(1)Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g),△H1=-25KJ/mol…①,
3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g),△H2=-47KJ/mol…②,
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g),△H3=19KJ/mol…③,
根据盖斯定律将方程式变形(3×①-②-2×③)÷6得:Fe(s)+CO(g)═Fe(s)+CO2(g),△H=$\frac{(3×△H1-△H2-2×△H3)}{6}$=-11KJ/mol.
故答案为:FeO(s)+CO(g)═Fe(s)+CO2(g)△H=-11KJ/mol;
(2)①依据题意,反应物为Co2+与肼(N2H4)、碱性条件下存在OH-,生成物为:钴单质,据此得出Co的化合价降低,故N的化合价升高,只能为0价,即氮气,据此得出还有水生成,氧化还原反应中存在得失电子守恒以及元素守恒,故此反应的离子反应方程式为:2Co2++N2H4+4OH-=2Co↓+N2↑+4H2O,
故答案为:2Co2++N2H4+4OH-=2Co↓+N2↑+4H2O;
②化学平衡状态,反应的正逆反应速率相同,各成分含量保持不变分析选项,3N2H4(g)$?_{△}^{催化剂}$N2(g)+4NH3(g)反应是气体体积变化的反应;
a.容器内压强不随时间改变,即各成分含量保持不变,能说明反应达到平衡状态,故a符合;
b.单位时间内生成amol N2的同时,生成4molNH3,都表示的是正反应,故不能说明正逆反应速率相同,不能说明反应达到平衡状态,故b不符合;
c.N2H4和NH3的物质的量之比保持不变,即各成分含量保持不变,故c符合;
d.混合气体的平均摩尔质量保持不变的前提是气体组成不变,故反应到达了平衡,故d符合;
故选acd;曲线b表示的是NH3的体积分数随温度的变化情况;为抑制肼的分解,可采取的合理措施有降低反应温度或增加压强等;
故答案为:a c d;NH3;降低反应温度或增加压强等;
(3)①依据图示可知,二氧化硫被氧化为硫酸根,所以二氧化硫所在的区为阳极区,阳极区发生反应SO2-2e-+2H2O═SO42-+4H+,与电源的正极相连的a为阳极,故a为阳极,b为阴极,阴极的电极反应式为:2HSO3-+2H++2e-═S2O42-+2H2O,
故答案为:阳;2HSO3-+2H++2e-═S2O42-+2H2O;
②该装置吸收SO2的原理是SO2在 a极发生氧化反应,电极反应式:SO2-2e-+2H2O=4H++SO42-,H+通过阳离子交换膜进入b 极室,
故答案为:SO2在 a极发生氧化反应,电极反应式:SO2-2e-+2H2O=4H++SO42-,H+通过阳离子交换膜进入b 极室.
点评 本题是综合性题目,关键是(3)考查了电解原理的分析应用,主要是电极反应,电极名称判断,理解电解池原理是关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
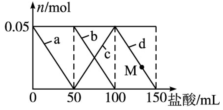 向100mL含Na2CO3、NaAlO2的混合溶液中逐滴加入150mL 1mol•L-1HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法正确的是( )
向100mL含Na2CO3、NaAlO2的混合溶液中逐滴加入150mL 1mol•L-1HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法正确的是( )| A. | a曲线表示的离子方程式为:AlO2-+H++H2O═Al(OH)3↓ | |
| B. | b曲线表示碳酸钠和盐酸反应,d曲线表示氢氧化铝的溶解 | |
| C. | M点时,溶液中沉淀的质量小于3.9 g | |
| D. | 原混合溶液中的Na2CO3溶液的浓度为1 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
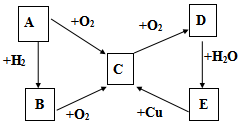 已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素.
已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
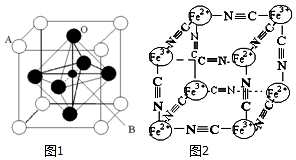
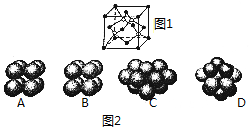 (1)碳化硅的晶胞结构(如图1)与金刚石类似(其中“●”为碳原子,“○”为硅原子).图2中“●”点构成的堆积方式与下列图示中D所表示的堆积方式相同
(1)碳化硅的晶胞结构(如图1)与金刚石类似(其中“●”为碳原子,“○”为硅原子).图2中“●”点构成的堆积方式与下列图示中D所表示的堆积方式相同查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Ti、Fe、Cr、Mn等均为过渡元素,在生产生活中起着不可替代的重要作用,对其单质和化合物的应用研究是目前科学研究的前沿之一.请回答下列问题:
Ti、Fe、Cr、Mn等均为过渡元素,在生产生活中起着不可替代的重要作用,对其单质和化合物的应用研究是目前科学研究的前沿之一.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | W与X形成的简单二元化合物的电子式为 | |
| B. | 短周期元素中Y的原子半径最大 | |
| C. | 工业上通过电解Y的氧化物制取Y的单质 | |
| D. | 最外层电子数等于其电子层数的金属与Z形成离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
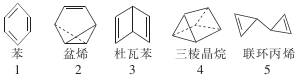 在探索苯结构的过程中,人们写出了符合分子式“C6H6”的多种可能结构(如图),下列说法正确的是( )
在探索苯结构的过程中,人们写出了符合分子式“C6H6”的多种可能结构(如图),下列说法正确的是( )| A. | 1~5对应的结构均能与氢气在一定条件下发生加成反应 | |
| B. | 1~5对应的结构中的一氯取代物只有1种的有3个 | |
| C. | 1~5对应的结构中所有原子均可能处于同一平面的有1个 | |
| D. | 1~5对应的结构中能使溴的四氯化碳溶液褪色的有4个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C4H6和C5H8的烃 | B. | 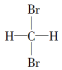 和 和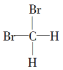 | ||
| C. | 符合CnH2n通式的烃 | D. | 分子式为C4H10和C20H42的烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
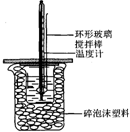 50mL 1.0mol•L-1盐酸跟50mL 1.1mol•L-1氢氧化钠溶液在图所示装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热.试回答下列问题:
50mL 1.0mol•L-1盐酸跟50mL 1.1mol•L-1氢氧化钠溶液在图所示装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热.试回答下列问题:| 实验序号 | 起始温度t1/℃ | 终止温度/t2/℃ | 温差(t2-t1)/℃ |
| 1 | 25.0 | 32.6 | |
| 2 | 25.1 | 31.8 | |
| 3 | 25.1 | 31.9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com