
【题目】常温下,浓度均为![]() 、体积均为
、体积均为![]() 的NaX、NaY溶液分别加水稀释至体积为
的NaX、NaY溶液分别加水稀释至体积为![]() 与
与![]() 的变化关系如图所示。已知
的变化关系如图所示。已知![]() 。下列说法不正确的是( )
。下列说法不正确的是( )

A.水的电离程度a点大于b点
B.HX、HY都是弱酸,且![]()
C.![]() 时,NaX溶液所含离子总数大于NaY溶液
时,NaX溶液所含离子总数大于NaY溶液
D.分别向稀释前的两种溶液中加入盐酸至![]() ,
,![]()
【答案】D
【解析】
A.NaX、NaY溶液水解溶液呈碱性,促进了水的电离,溶液碱性越强,水的电离程度越大,根据![]() 可知,pOH越大溶液碱性越弱,根据图象可知,pOH:
可知,pOH越大溶液碱性越弱,根据图象可知,pOH:![]() ,则水的电离程度a点大于b点,故A正确;
,则水的电离程度a点大于b点,故A正确;
B.图象可知NaX、NaY溶液pOH大小![]() ,说明碱性
,说明碱性![]() ,当
,当![]() 时,NaY溶液pOH变化大,说明
时,NaY溶液pOH变化大,说明![]() 离子水解程度大,对应酸的酸性
离子水解程度大,对应酸的酸性![]() ,酸性越强电离平衡常数越大,则电离平衡常数:
,酸性越强电离平衡常数越大,则电离平衡常数:![]() ,故B正确;
,故B正确;
C.当![]() 时,NaY溶液的pOH较小,则说明
时,NaY溶液的pOH较小,则说明![]() 离子水解程度较大,NaX溶液中电荷守恒
离子水解程度较大,NaX溶液中电荷守恒![]() ,NaY溶液中电荷守恒
,NaY溶液中电荷守恒![]() ,两溶液中阳离子总浓度为
,两溶液中阳离子总浓度为![]() ;由于NaX溶液中
;由于NaX溶液中![]() 小于NaY溶液中
小于NaY溶液中![]() ,则
,则![]() :
:![]() ,两溶液中
,两溶液中![]() 相同,则NaX溶液中所含离子总数大于NaY溶液,故C正确;
相同,则NaX溶液中所含离子总数大于NaY溶液,故C正确;
D.向稀释前的两溶液中分别加盐酸至![]() 时,根据电荷守恒可知:
时,根据电荷守恒可知:![]() 、
、![]() ,盐溶液的pOH:
,盐溶液的pOH:![]() ,反应后溶液为中性时,NaY溶液消耗盐酸多,反应后溶液中
,反应后溶液为中性时,NaY溶液消耗盐酸多,反应后溶液中![]() :
:![]() ,则
,则![]() ,故D错误;
,故D错误;
答案选D。


 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
【题目】某温度下,![]() 和
和![]() 的电离常数分别为
的电离常数分别为![]() 和
和![]() 。将
。将![]() 和体积均相同的两种酸溶液分别稀释,其
和体积均相同的两种酸溶液分别稀释,其![]() 随加水体积的变化如图所示。下列叙述正确的是( )
随加水体积的变化如图所示。下列叙述正确的是( )

A. 曲线Ⅰ代表![]() 溶液
溶液
B. 溶液中水的电离程度:b点>c点
C. 从c点到d点,溶液中 保持不变(其中
保持不变(其中![]() 、
、![]() 分别代表相应的酸和酸根离子)
分别代表相应的酸和酸根离子)
D. 相同体积a点的两溶液分别与![]() 恰好中和后,溶液中
恰好中和后,溶液中![]() 相同
相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述正确的是( )
A.铁屑、溴水、苯混合加热就能制取溴苯
B.用苯、浓硫酸、浓硝酸制取硝基苯时,温度越高反应越快,得到的硝基苯越多
C.乙醇与乙酸混合加热即能发生酯化反应生成有香味的酯
D.![]() 过程中反应①、②分别是取代反应、加成反应
过程中反应①、②分别是取代反应、加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10 mol·L-1 KOH溶液滴定10.00 mL 0.10 mol·L-1 H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成两者溶液的体积之和),下列说法正确的是( )
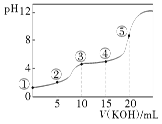
A.点②所示溶液中:c(K+)+c(H+)=c(HC2O4-)+c(C2O42-)+c(OH-)
B.点③所示溶液中:c(K+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-)
C.点④所示溶液中:c(K+)+c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.10 mol·L-1
D.点⑤所示溶液中:c(OH-)= c(H+)+ c(HC2O4-)+ c(C2O42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用如图所示装置进行有关实验:

(1)B是用来收集实验中产生的气体的装置,但未将导管画全,请在图上把导管补充完整_________。
(2)实验中他们取6.4 g铜片和12 mL 18 mol·L1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①写出铜跟浓硫酸反应的化学方程式:__________________;
②为什么有一定量的余酸但未能使铜片完全溶解,你认为原因是__________________;
③下列药品中能够用来证明反应结束后的烧瓶中确有余酸的是________(填编号)。
A.铁粉 B.BaCl2溶液 C.银粉 D.Na2CO3溶液
(3)装置C中试管D内盛装的是品红溶液,当B中气体收集满后,有可能观察到的现象是_____________,待反应结束后,向C中烧杯内加入沸水,D中观察到的现象是_____________。
(4)实验装置C有可能造成环境污染,试用最简单的方法加以解决,__________________(实验用品自选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中含有丰富的化学元素,图1是某化工厂从海水中提取![]() 、
、![]() (海水中以
(海水中以![]() 形式存在)、
形式存在)、![]() (海水中以
(海水中以![]() 形式存在)等物质的生产流程简图:
形式存在)等物质的生产流程简图:
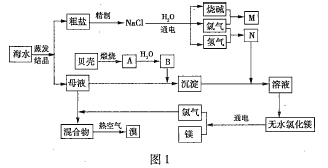
(1)![]() 中加入盐酸后,要获得
中加入盐酸后,要获得![]() 晶体,需要进行的实验操作依次为________(填序号)。
晶体,需要进行的实验操作依次为________(填序号)。
A 蒸馏 B 灼烧 C 过滤 D 蒸发 E 冷却结晶
(2)利用![]() 可制得无水氯化镁,应采取的措施是__________。
可制得无水氯化镁,应采取的措施是__________。
(3)母液中常含有![]() 、
、![]() 、
、![]() 、
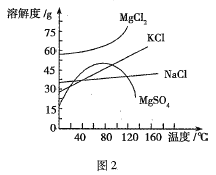
、![]() (各物质的溶解度曲线如图2所示)等,进一步加工可制得一些重要的产品。若将母液加热到60℃以上,随着水分的蒸发,会逐渐析出晶体,该晶体的主要成分有________、________;过滤上述晶体后,将滤液降温到30℃以下,又逐渐析出晶体,用一定量的冷水洗涤该晶体,最后可得到比较纯净的________晶体。
(各物质的溶解度曲线如图2所示)等,进一步加工可制得一些重要的产品。若将母液加热到60℃以上,随着水分的蒸发,会逐渐析出晶体,该晶体的主要成分有________、________;过滤上述晶体后,将滤液降温到30℃以下,又逐渐析出晶体,用一定量的冷水洗涤该晶体,最后可得到比较纯净的________晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NaOH溶液滴入某一元酸(HA)溶液中,测得混合溶液的pH与离子浓度变化关系如图所示[已知:![]() ]。下列叙述不正确的是
]。下列叙述不正确的是

A. Ka(HA)的数量级为10-5
B. 滴加NaOH溶液的过程中,![]() 保持不变
保持不变
C. m点所示溶液中:c(H+)+c(Na+)=c(HA)+c(OH-)
D. n点所示溶液中:c(Na+)=c(A-)+c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NaOH溶液分别加到HA、HB两种弱酸溶液中,两溶液中pH与粒子浓度比值的对数关系如图所示,已知![]() ,下列有关叙述错误的是( )
,下列有关叙述错误的是( )

A.HA、HB两种酸中,HB的酸性弱于HA
B.b点时,![]()
C.同浓度同体积的NaA和NaB溶液中,阴离子总数相等
D.向HB溶液中加入NaOH溶液所得的混合溶液中,
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体混合物可能由SiO2、Fe2O3、Fe、Na2SO3、Na2CO3、BaCl2中的两种或两种以上的物质组成。某兴趣小组为探究该固体混合物的组成,设计的部分实验方案如下图所示:

下列说法正确的是( )
A. 气体A是SO2和CO2的混合气体
B. 固体A一定含有SiO2,可能含有BaSO4
C. 该固体混合物中Fe2O3和Fe至少有其中一种
D. 该固体混合物一定含有Fe、Na2SO3、BaCl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com