
| A£®Ca(ClO)2£¾FeCl3£¾Cl2£¾I2 | B£®Cl2£¾ Ca(ClO)2£¾ FeCl3£¾I2 |
| C£®Ca(ClO)2£¾Cl2£¾FeCl3£¾I2 | D£®Ca(ClO)2£¾Cl2£¾I2£¾FeCl3 |
 ÖÜÖÜĒå¼ģ²āĻµĮŠ“š°ø
ÖÜÖÜĒå¼ģ²āĻµĮŠ“š°ø ĒįĒɶį¹ŚÖܲāŌĀæ¼Ö±ĶØøßæ¼ĻµĮŠ“š°ø
ĒįĒɶį¹ŚÖܲāŌĀæ¼Ö±ĶØøßæ¼ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗŹµŃéĢā

| | ŹµŃé²Ł×÷ | ŹµŃéĻÖĻó |
| I | “ņæŖ»īČūa£¬µĪ¼ÓĀČĖ®£¬¹Ų±Õ»īČūa | AÖŠČÜŅŗ±äĪŖŗģ×ŲÉ«”£ |
| II | “µČėČČæÕĘų | AÖŠŗģ×ŲÉ«Ć÷ĻŌ±äĒ³£»BÖŠÓŠĘųÅŻ£¬²śÉś“óĮæ°×É«³Įµķ£¬»ģŗĻŅŗŃÕÉ«ĪŽĆ÷ĻŌ±ä»Æ”£ |
| III | Ķ£Ö¹“µČėæÕĘų£¬“ņæŖ»īČūb£¬ÖšµĪ¼ÓČėH2O2ČÜŅŗ | æŖŹ¼Ź±ŃÕÉ«ĪŽĆ÷ĻŌ±ä»Æ£»¼ĢŠųµĪ¼ÓH2O2ČÜŅŗ£¬Ņ»¶ĪŹ±¼äŗ󣬻ģŗĻŅŗÖš½„±ä³Éŗģ×ŲÉ«”£ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ClO3-£¾BrO3-£¾Cl2£¾Fe3+£¾I2 | B£®BrO3-£¾Cl2£¾ClO3-£¾I2£¾Fe3+ |
| C£®BrO3-£¾ClO3-£¾Cl2£¾Fe3+£¾I2 | D£®BrO3-£¾ClO3-£¾Fe3+£¾Cl2£¾I2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ca(ClO)2 | B£®NaOH | C£®FeSO4 | D£®Na2SO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ńõ»ÆŠŌ£ŗA2£¾B2£¾C2£¾D2 | B£®»¹ŌŠŌ£ŗA-£¾B-£¾C-£¾D- |
| C£®2A-+D2=2D-+A2·“Ó¦æÉŅŌ½ųŠŠ | D£®2C-+B2=2B-+C2·“Ó¦²»ÄܽųŠŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ńõ»ÆŠŌ: I2>Br2 >Cl2 | B£®Ńõ»ÆŠŌ: Br2 >I2>Cl2 |
| C£®Ńõ»ÆŠŌ: Cl2 > Br2 > I2 | D£®Ńõ»ÆŠŌ: I2>Cl2 >Br2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
A£®2Fe3£«£«SO2£«2H2O = 2Fe2£«£«SO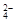 £«4H£« £«4H£« | B£®I2£«SO2£«2H2O = H2SO4£«2HI |
| C£®H2O2£«H2SO4 = SO2”ü£«O2”ü£«2H2O | D£®2Fe2£«£«Cl2 = 2Fe3£«£«2Cl£ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Fe3+ Cl2 I2 | B£®Cl2 Fe3+ I2 |
| C£®I2 Cl2 Fe3+ | D£®Cl2 I2 Fe3+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®H2S>H2SO3>I”Ŗ>Br”Ŗ | B£®Br”Ŗ>I”Ŗ>H2SO3>H2S |
| C£®H2SO3>H2S>Br”Ŗ>I”Ŗ | D£®I”Ŗ>Br”Ŗ>H2S>H2SO3 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com