
【题目】有机物A、B、C结构如下:
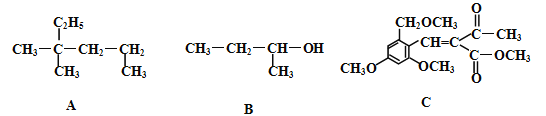
(1)A分子的主链上有 个碳原子 ;若A是某单烯烃与H2发生加成反应后得到的产物,符合此条件的单烯烃有 种。
(2)B在常温下呈 态;B的系统命名法名称是 。
(3)C的分子式是 ,向C中滴入溴水时,1molC能与 molBr2发生加成。
(4)关于A、B、C三种物质的下列说法中不正确的是 。
a.都能发生氧化反应
b.都能发生消去反应
c.都能发生取代反应
d.都能发生聚合反应
【答案】(1)6;3.(2)液;2-丁醇 (3)C16H20O6,1。 (4)bd(本空2分)
【解析】
试题分析:(1)根据A的结构简式可知A分子的主链上有6个碳原子;若A是某单烯烃与H2发生加成反应后得到的产物,则相应的烷烃分子中相邻两个碳原子个去掉一个氢原子即可形成碳碳双键,因此符合此条件的单烯烃有3种。
(2)B是2-丁醇,在常温下呈液态。
(3)根据C的结构简式可知C的分子式是C16H20O6,C分子中含有1个碳碳双键,则向C中滴入溴水时,1molC能与1molBr2发生加成。
(4)a.三种物质都燃烧,均都能发生氧化反应,a正确;b.只有2-丁醇能发生消去反应,b错误;c.三种都能发生取代反应,c正确;d.只有C物质能发生聚合反应,d错误,答案选bd。


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
【题目】实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:
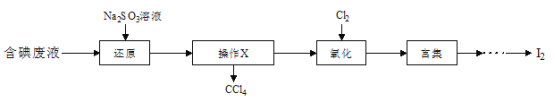
(1)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为_____________________;该操作将I2还原为I-的 目的是__________________。
(2)操作X的名称为 ________________。
(3)氧化时,在三颈烧瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在40℃左右反应(实验装置如右图所示)。实验必须控制在较低温度下进行的原因是 ;仪器a、b的名称分别为:a__________、b__________;仪器b中盛放的溶液为__________________。

(4)已知二氧化氯为黄绿色易溶于水的气体,是高效、低毒的消毒剂和水处理剂。现用ClO2氧化酸性含I-废液以回收碘。
①写出ClO2氧化I-的离子方程式 ;
②若处理含相同物质的量的I-酸性废液以回收碘,所需Cl2的物质的量是ClO2的_________倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(5分)由含铜废料制铜的一种方案是:
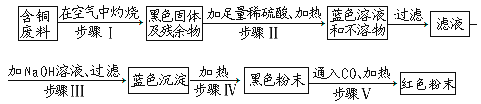
(1)写出下列步骤中的化学方程式:步骤Ⅲ:_________.步骤V:_________.
(2)步骤Ⅱ后形成的蓝色溶液中的溶质是_________.
(3)上述方案中可能造成空气污染的步骤是_________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、R、Q、M是六种短周期元素,原子序数依次增大。X是原子半径最小的元素,Y的气态氢化物能使湿润的红色石蕊试纸变蓝,Z为地壳中含量最多的元素,R与X同主族;Y、R、Q最外层电子数之和为8,M的单质黄绿色有害气体。请回答下列问题:
(1)R在元素周期表中的位置为___________。
(2)Z、Q、M简单离子半径由大到小的顺序为(写元素离子符号)___________。
(3)X、Y、Z三种元素形成盐类化合物的水溶液呈酸性的原因:(用离子方程式表示)________________。
溶液中所含离子浓度由大到小的顺序为________________。
(4)YX4M的电子式为___________,Q3Y2与水可剧烈反应,产生沉淀与气体,反应的化学方程式为
____________________。
(5)X、Z两元素形成的原子个数比为1:1的化合物中含有的化学键类型为_______________________。
(6)M的单质与R的最高价氧化物对应的水化物反应的离子方程式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯环结构中,不存在单双键交替结构,可以作为证据的事实是
①苯不能使酸性KMnO4溶液褪色;
②苯中碳碳键的键长均相等;
③苯能在一定条件下跟H2加成生成环己烷;
④经实验测得邻二甲苯(![]() )仅一种结构;
)仅一种结构;
⑤苯在FeBr3存在的条件下同液溴可发生取代反应,但不能因化学变化而使溴水褪色。
A. ③④⑤ B. ①③④ . C. ①②④⑤ D. ①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com