
【题目】下列除去括号内的杂质选用的试剂及方法均正确的是( )
序号 | 被提纯的物质 | 除杂试剂 | 分离方法 |
A | 溴化钠溶液(碘化钠) | 氯水、四氯化碳 | 萃取、分液 |
B | 碳酸氢钠溶液(碳酸钠) | 石灰水 | 过滤 |
C |
| 碳酸钠溶液 | 洗气 |
D | 酒精(水) | 生石灰 | 蒸馏 |
A. AB. BC. CD. D
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:
CO(g)+H2S(g)![]() COS(g)+H2(g) K=0.1
COS(g)+H2(g) K=0.1
反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是
A. 升高温度,H2S浓度增加,表明该反应是吸热反应
B. 通入CO后,正反应速率逐渐增大
C. 反应前H2S物质的量为7mol
D. CO的平衡转化率为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜铁是目前人们使用量最大的合金材料,铁及其化合物也是人们日常生活中应用广泛的一类物质。回答下列问题:
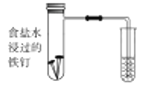
(1)下图中铁钉发生的电化学腐蚀类型是________,负极反应式为__________。
(2)实验室配置![]() 溶液时,需向溶液中滴加几滴稀硫酸,其目的是__________,
溶液时,需向溶液中滴加几滴稀硫酸,其目的是__________,![]() 溶液中离子浓度由大到小的顺序是________。
溶液中离子浓度由大到小的顺序是________。
(3)高铁盐酸是一种新型的环境消毒剂及水体净化剂,如高铁酸钾(![]() )。其中
)。其中![]() 的化合价是________,其净水过程中既表现出强氧化性,又表现了强吸附性,则
的化合价是________,其净水过程中既表现出强氧化性,又表现了强吸附性,则![]() 与水反应的离子方程式为__________。
与水反应的离子方程式为__________。
(4)羰基铁酸[![]() ]是一种二元弱酸,其第一步电离方程式为__________。
]是一种二元弱酸,其第一步电离方程式为__________。
(5)25℃时,向含![]() 的溶液中加入一定量的
的溶液中加入一定量的![]() 后,
后,![]() 恰好达到溶液平衡,测得溶液的
恰好达到溶液平衡,测得溶液的![]() ,
,![]() 。通过计算判断所得的
。通过计算判断所得的![]() 中是否含有
中是否含有![]() 杂质:________(已知:
杂质:________(已知:![]() ,
,![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案与现象正确且能达到相应实验目的的是( )
选项 | 实验目的 | 实验方案与现象 |
A | 证明新制氯水具有酸性 | 向新制氯水中滴加紫色石蕊试液,溶液变为红色且颜色保持不变 |
B | 证明酸性条件下,氧化性:H2O2 > Fe3 + | 向Fe(NO3)2溶液中滴加用硫酸酸化的H2O2溶液,溶液变黄色 |
C | 证明同温下,溶度积常数: Ksp(AgCl)> Ksp(Ag2CrO4) | 向体积为100 mL、浓度均为0.01 mol·L-1的NaCl和Na2CrO4混合溶液中滴加 0.01 mol·L-1AgNO3溶液,先产生白色沉淀,后产生砖红色沉淀Ag2CrO4 |
D | 证明溶液X中含有 | 向溶液X中先滴加盐酸无明显现象,再滴加BaCl2溶液,出现白色沉淀 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在指定条件和相应的计量下,甲物质能与乙物质恰好都能完全反应的是
选项 | 甲 | 乙 | 条件 |
A | 1L0.4 mol·L-1氨水 | 含0.12molAlCl3的AlCl3溶液 | 常温常压 |
B | 0.9g Al | 50 mL18.4 mol·L-1H2SO4溶液 | 常温 |
C | 2.24L SO2 | 含0.1molNaOH的NaOH溶液 | 标准状况 |
D | 1mL Cl2 | 5mL H2O | 常温、避光 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X、Y、Z和W在周期表中的位置如图所示,其中X、Y、Z均为短周期元素,且X、Y、W原子的最外层电子数之和为13。下列说法不正确的是( )
X | Y | ||
Z | |||
W |
A. 原子半径:![]()
B. W的最高价氧化物对应的水化物可能为强碱
C. 上述四种元素可形成化合物![]()
D. 一定条件下,Z单质与X的氢化物及Y的氢化物均能反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某中学化学课外兴趣小组通过实验探究Fe2+、Fe3+的性质。回答下列问题:
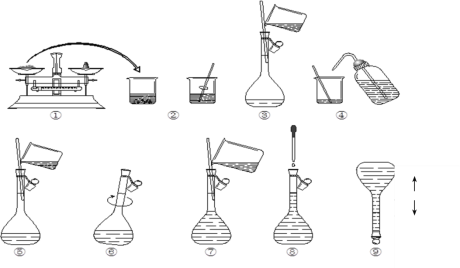
(1)本次实验中共需要1mol/LFeCl2溶液100 mL,配制时涉及到如下操作:
①步骤③中玻璃棒的作用是__;
②在配制溶液过程中步骤⑦所进行的操作是___(填“洗涤”、“转移”、“定容”);该步中视线应与溶液凹液面的最低处保持___。
③下列操作会使所配溶液物质的量浓度偏低的是___。
A.溶解后小烧杯、玻璃棒没有洗涤
B.所用容量瓶中,已有少量蒸馏水
C.定容、加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度线
(2)取2mLFeCl2溶液于试管中,加入几滴氯水,再加入1滴KSCN溶液,观察到的现象为__,说明Cl2可将Fe2+氧化成Fe3+。FeCl2溶液与氯水反应的离子方程式为___,此时将所取FeCl2溶液完全反应需__molCl2。
(3)在(2)溶液中加入过量的铁粉,溶液变成___色;发生反应的离子方程式为__,此时溶液中所含铁元素的微粒的物质的量为__mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用KMnO4和浓盐酸反应制取氯气,其变化可表述为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl↑2+8H2O。
(1)请将上述化学方程式改写为离子方程式:__。
(2)浓盐酸在反应中显示出来的性质是__(填编号)。
①只有还原性②还原性和酸性③只有氧化性④氧化性和酸性
(3)此反应中氧化产物是Cl2,若产生0.5molCl2,则转移电子的物质的量为__mol。
(4)用双线桥法表示该反应电子转移的方向和数目__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以含镍废硫酸盐(含 Ni2+ 、Fe2+ 、Cu2+ 、Co2+ 、A13+ 、Mn2+ 、Cr3+ 、Mg2+ 、Zn2+ 等)为原料制取NiSO4·6H2O 的工艺流程如下:
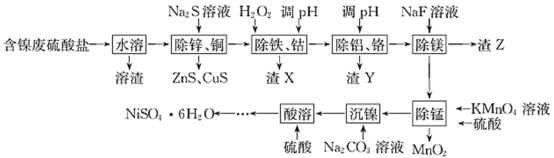
相关金属离子形成氢氧化物沉淀的pH 范围如下:
金属离子 | Co2+ | Co3+ | Fe2+ | Fe3+ | A13+ | Cr3+ | Ni2+ |
开始沉淀的pH | 7.2 | 0.23 | 6.3 | 1.5 | 4.1 | 4.3 | 6.9 |
沉淀完全的pH | 9.2 | 1.1 | 8.3 | 2.8 | 5.4 | 5.6 | 8.9 |
回答下列问题:
(1)已知1gKsp(CuS)= -47.6,1gKsp(ZnS)= -23.8,则反应ZnS+Cu2+![]() CuS+Zn2+的平衡常数对数值1gK= ________________________。
CuS+Zn2+的平衡常数对数值1gK= ________________________。
(2)“除铁、钴”时,加入H2O2的目的是 ______________,得到的渣X为________。
(3) “除铝、铬”时,调pH 范围为 _________;滤渣Y 中含Cr(OH)3,其性质与 A1(OH)3 类似,写出Cr(OH)3与NaOH反应的化学方程式: __________________。
(4)“除锰”时,发生反应的离子方程式为___________________________。
(5)“酸溶”得到溶液制备 NiSO4·6H2O晶体,还需进行的操作工艺是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com