
下列说法中错误的是
A.从1 L 1mol·L-1的NaCl溶液中取出10 mL,其浓度仍是1mol·L-1
B.制成0.5L 10mol·L-1的盐酸,需要氯化氢气体112L(标准状况)
C.0.5L 2mol·L-1 BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023
D.10g 98%的硫酸溶液(密度为1.84 g·cm-3)与10 mL 18.4mol·L-1的硫酸溶液的浓度不相同
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源:2015-2016学年江西省高二上学期12月月考化学试卷(教师版) 题型:选择题
下列自发反应可用能量判据来解释的是
A.2H2(g)+O2(g)=2H2O(l) ΔH =-285.8kJ/mol
B.2N2O5(g)=4NO2(g)+O2(g) ΔH =+56.7kJ/mol
C.(NH4)2CO3(s) =NH4HCO3(s)+NH3(g) ΔH =+74.9kJ/mol
D.硝酸铵自发地溶于水
查看答案和解析>>
科目:高中化学 来源:2016届西藏自治区拉萨中学高三上学期第四次月考化学试卷(解析版) 题型:推断题
A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系: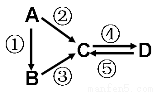
(1)若B是淡黄色固体,②③反应均用到同一种液态氢化物。D物质常用于食品工业。写出④反应的化学方程式 ;
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。写出③反应的化学方程式 ;
(3)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。写出④反应离子方程式 ;
(4)若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中除钠、氧外的元素为同一主族,且溶液均显碱性。写出②反应的化学方程式 ;
(5)若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种非金属单质。写出④反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三上学期月考化学试卷(解析版) 题型:选择题
已知NaHSO3溶液显酸性,溶液中存在以下平衡:
HSO3-+ H2O  H2SO3 + OH- ①
H2SO3 + OH- ①
HSO3- H+ + SO32- ②
H+ + SO32- ②
向0.1mol·L-1的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是
A.加入少量固体NaOH,平衡①左移,平衡②右移,溶液中c(HSO3-)增大
B.加入等体积等浓度Na2SO3溶液,则3c(Na+) = 2[c(HSO3-) + c(H2SO3) +c(SO32-)]
C.加入少量NaOH溶液, 、
、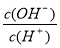 的值均增大
的值均增大
D.加入氨水至中性,则2c(Na+) = c(SO32-)>c(H+) = c(OH-)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一上期末模拟化学试卷(解析版) 题型:选择题
下列由相关实验现象所推出的结论正确的是
A.向某溶液中加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,则该溶液一定含有SO42-
B.向某溶液中加入CCl4,CCl4层显紫色,证明原溶液中存在I2
C.向某溶液中加入稀盐酸,产生的气体能使澄清石灰水变浑浊,则溶液中一定含有CO32-
D.向一定浓度的Na2SiO3溶液中通入适量CO2气体,出现白色沉淀,说明H2SiO3的酸性强于H2CO3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上第三次月考化学试卷(解析版) 题型:选择题
已知某温度下CH3COOH和NH3•H2O 的电离常数相等,现向10mL浓度为0.1mol•L?1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中
A.水的电离程度始终增大
B.c(NH4+)/c(NH3•H2O)先增大再减小
C.c(CH3COOH)与c(CH3COO?)之和始终保持不变
D.当加入氨水的体积为10mL时,c(NH4+)=c(CH3COO?)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上期中考试化学试卷(解析版) 题型:选择题
关于浓度的关系,下列说法错误的是
A.等浓度的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-)
B.新制氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-)
C.室温下,向0.01mol/LNH4HSO4溶液中滴加NaOH溶液至中性:
c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)>c(ClO-)
D.物质的量浓度均为 的
的 和
和 混合溶液中,浓度可能的关系为:
混合溶液中,浓度可能的关系为:
c(Na+)>c(OH-)>c(HA)>c(HB)
查看答案和解析>>
科目:高中化学 来源:2016届宁夏固原一中高三上适应性训练理综化学试卷(解析版) 题型:推断题
从海水中提取一些重要的化工产品的工艺流程如图所示。

根据上述流程图回答下列问题:
(1)图中A的化学式为____________,在制取A的过程中需向饱和NaCl溶液中先后通入两种气体,后通入气体的化学式为_____________________。
(2)海水淡化处理的方法有______________________________。(写出3种即可)
(3)过程⑤的化学方程式为_________________________。
(4)从B溶液制备B的无水晶体的“操作a”为_____________________。
(5)过程③用SO2水溶液吸收溴单质,吸收率可达93%,生成两种强酸,写出反应的离子方程式 ______________________________。
(6)过程②到过程④的变化为“Br-→Br2→Br-→Br2”,其目的是_____ 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高二上学期12月月考化学试卷(解析版) 题型:选择题
已知铝与O2、O3在一定条件下均能反应,且都生成Al2O3。反应的热化学方程式如下:
4Al(s)+ 3O2(g)===2Al2O3(s);△H=-Q1 kJ/mol
4Al(s)+ 2O3(g)===2Al2O3(s);△H=-Q2 kJ/mol。
已知:Q1 、Q2均大于0,且Q1 <Q2,下列说法正确的组合是
①上述两个反应均为吸热反应; ②4mol固态Al和3mol气态O2所具有的总能量大于2mol固态Al2O3所具有的能量;③等质量的O2 、O3,O2的能量高; ④等物质的量的O2 、O3,O3的能量高;⑤由O2生成O3的反应为放热反应; ⑥由O2生成O3的反应为吸热反应;
A.①②④ B.②④⑥ C.②③⑤ D.③④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com