
| A. | HCl、H2SO4、NaOH | B. | NaOH、HCl、H2SO4 | ||
| C. | HCl、H2SO4、NH3•H2O | D. | HCl、NH3•H2O、H2SO4 |
科目:高中化学 来源: 题型:解答题
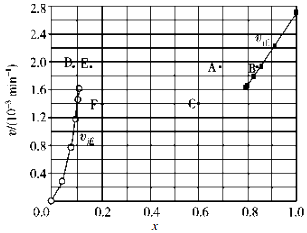 (1)已知反应 2HI(g)?H2(g)+I2(g)的△H=+11kJ/mol,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1mol HI(g)分子中化学键断裂时需吸收的能量为299kJ.
(1)已知反应 2HI(g)?H2(g)+I2(g)的△H=+11kJ/mol,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1mol HI(g)分子中化学键断裂时需吸收的能量为299kJ.| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
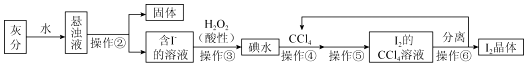
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气是一种紫色重要的化工原料 | |
| B. | 钠和钾的合金在常温下是固体 | |
| C. | 用二氧化硅具有很强的导光能力,可用于制作光缆 | |
| D. | 发酵粉中含有碳酸钠,能使焙制出的糕点疏松多孔 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某烷烃的命名为:2-甲基-3-乙基丁烷 | |
| B. | 分子式为 C4H8O2的酯有 4 种 | |
| C. | 乙烯分别使溴水和酸性 KMnO4 溶液褪色,反应类型相同 | |
| D. | 油脂是能发生水解反应的高分子化合物 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一上10月月考化学试卷(解析版) 题型:选择题
下列溶液中,K+的物质的量浓度最大的是( )
A.0.1 mol/L的KNO3 溶液500 ml B.0.05mol/L的K2SO4 溶液300ml
C.0.04mol/L的K3PO4 溶液100 ml D.0.06mol/L的KHCO3 溶液120 ml
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,pH=2的1.0 L H2SO4溶液中含有H+的数目为0.02 NA | |
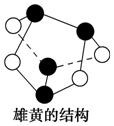
| B. | 0.5 mol雄黄(As4S4,所有原子都满足8电子结构,结构如图)含有NA个S-S键 | |
| C. | 39 g苯分子中共含6 NA个共价单键 | |
| D. | 向FeI2、NaBr的混合溶液中通入适量氯气,当有1 molFe2+被氧化时,该反应转移电子的数目至少为3 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com