


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:
 反应的H2或溴水中Br2的最大量分别是( )
反应的H2或溴水中Br2的最大量分别是( )| A、11mol,9mol |
| B、9 mol,6mol |
| C、6mol,5 mol |
| D、l3 mol,9mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
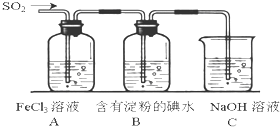 某校化学兴趣小组为探究SO2气体的还原性设计了如下装置图:
某校化学兴趣小组为探究SO2气体的还原性设计了如下装置图:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 物质 | 杂质 | 除杂质应选用的试剂或操作方法 |
| ① | KNO3溶液 | KOH | 加入FeCl3溶液,并过渡 |
| ② | Al2(SO4)3溶液 | MgSO4 | 加入过量烧碱后过滤,再用硫酸酸化滤液 |
| ③ | CO2 | SO2 | 通过盛KMnO4(H+)溶液烧洗气瓶,再通过浓硫酸的洗气瓶 |
| ④ | NaNO3 | CaCO3 | 溶解、过滤、蒸发结晶 |
| A、①②④ | B、③④ |
| C、②③④ | D、①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、熔融状态下该晶体能导电 |
| B、K3C60中碳元素显-3价 |
| C、K3C60中只有离子键 |
| D、C60与12C互为同素异形体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com