

分析 (1)二氧化锰与浓盐酸反应生成氯气;
(2)干燥的氯气没有漂白性,次氯酸具有漂白性;氯气与NaOH反应生成NaCl和NaClO、水;
(3)Fe的金属性比Cu强,能与氯气反应生成氯化铁;
(4)K37ClO3+6H35Cl=K35Cl+35Cl37Cl↑+35Cl2↑+3H2O,据此分析;
(5)在酸性条件下,NaClO3和Na2SO3溶液混合反应生成ClO2.
解答 解:(1)二氧化锰与浓盐酸反应生成氯气,其反应的方程式为:MnO2+4HCl(浓)$\frac{\underline{\;△\;}}{\;}$MnCl2+Cl2↑+2H2O;
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;△\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)干燥的氯气没有漂白性,氯气与水发应生成次氯酸,次氯酸具有漂白性,所以b褪色;氯气与NaOH反应生成NaCl和NaClO、水,其反应的方程式为:Cl2+2NaOH═NaCl+NaClO+H2O;
故答案为:b;Cl2+2NaOH═NaCl+NaClO+H2O;
(3)将铜丝换成铁丝,做Ⅲ实验,结果也能点燃,因为Fe的金属性比Cu强,能与氯气反应生成氯化铁;
故答案为:D;
(4)K37ClO3+6H35Cl=K35Cl+35Cl37Cl↑+235Cl2↑+3H2O,反应产物中有一个35Cl37Cl和两个35Cl2,则氯气的平均相对分子质量是$\frac{35+37+35×4}{3}$=70.7;
故答案为:70.7;
(5)在酸性条件下,NaClO3和Na2SO3溶液混合反应生成ClO2,其反应方程式为:2NaClO3+Na2SO3+H2SO4═2ClO2↑+2NaSO4+H2O;
故答案为:2NaClO3+Na2SO3+H2SO4═2ClO2↑+2NaSO4+H2O.
点评 本题考查了气体的实验室制法、反应原理、物质的性质,题目难度中等,侧重于考查学生的实验能力和对基础知识的综合应用能力.


科目:高中化学 来源: 题型:解答题

 ;
; ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电力 | B. | 核能 | C. | 太阳能 | D. | 氢能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学键既存在于相邻原子间又存在于相邻分子间 | |
| B. | 两个原子间的相互作用叫化学键 | |
| C. | 化学键通常指的是相邻的两个或多个原子之间的强烈的相互作用 | |
| D. | 化学键的实质是静电吸引 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ | |
| B. | 氢氧化钡与稀硫酸混合:SO42-+H++OH-+Ba2+=H2O+BaSO4↓ | |
| C. | 用稀硫酸洗去铁锈:Fe2O3+6H+=2 Fe3++3H2O | |
| D. | 石灰乳与Na2CO3溶液混合:Ca2++CO32-=CaCO3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 压强/MPa G体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 83.0 |
| A. | 4个 | B. | 3个 | C. | 2个 | D. | 1个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 和
和
 和
和
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
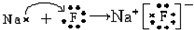 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 92.3% | B. | 87.6% | C. | 75% | D. | 84.9% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com