
| A. | 阳离子中一定含有金属元素 | |
| B. | 在氧化还原反应中,非金属单质一定是氧化剂 | |
| C. | 某元素从化合态变为游离态时,该元素一定被还原 | |
| D. | 金属阳离子被还原不一定得到金属单质 |
分析 A.阳离子中不一定含有金属元素,如铵根;
B.非金属单质可为氧化剂,也可为还原剂;
C.某元素从化合态变为游离态,化合价可能升高,也可能降低;
D.如金属有多种价态,被还原时可能由高价态生成低价态化合物.
解答 解:A.阳离子中不一定含有金属元素,如NH4+,故A错误;
B.非金属单质可为氧化剂,也可为还原剂,如氯气与水或碱的反应中,Cl元素的化合价既升高又降低,故B错误;
C.某元素从化合态变为游离态,化合价可能升高,也可能降低,如S2-→S为被氧化过程,Fe2+→Fe为被还原过程,故C错误;
D.如金属有多种价态,被还原时可能由高价态生成低价态化合物,如Fe3+→Fe2+,故D正确.
故选D
点评 本题考查氧化还原反应,为高频考点,侧重于学生的分析能力的考查,注意把握相关基础知识的积累,解答时注意能找出反例,难度不大.


科目:高中化学 来源: 题型:选择题
 已知:还原性HSO3->I-,氧化性IO3->I2.在含3molNaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列不正确的是( )
已知:还原性HSO3->I-,氧化性IO3->I2.在含3molNaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列不正确的是( )| A. | 0~b间的反应可用离子方程式表示:3HSO3-+IO3-=3SO42-+I-+3H+ | |
| B. | a点时消耗NaHSO3的物质的量为1.2 mol | |
| C. | b点到c点,KIO3与NaHSO3反应生成I2 | |
| D. | 当溶液中I-与I2的物质的量之比为5:2,加入的KIO3为1.08 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 | |
| B. | 浓硝酸在光照条件下颜色变黄,说明浓硝酸不稳定 | |
| C. | 常温下浓硫酸、浓硝酸可以用铝罐储存,说明浓硫酸、浓硝酸与铝不反应 | |
| D. | 反应CuSO4+H2S═CuS↓+H2SO4说明硫化铜既不溶于水,也不溶于稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 反应前后各元素的化合价均不变 | |
| B. | 水煤气的成分是一氧化碳和氧气 | |
| C. | 该反应中含氢元素的化合物有3种 | |
| D. | 该反应的化学方程式中甲烷和水的计量数之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④①②③ | B. | ①③④② | C. | ④③②① | D. | ①④②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、H+、SO42-、OH- | B. | Na+、Cu2+、NO3-、Cl- | ||
| C. | H+、Ca2+、Cl-、NO3- | D. | Ag+ Na+、NO3-、Cl-、 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 甲烷分子中的4个氢原子都可以被取代,若甲烷分子中的4个氢原子都被苯基取代,可以得到的分子如图,对该分子的描述,不正确的是( )
甲烷分子中的4个氢原子都可以被取代,若甲烷分子中的4个氢原子都被苯基取代,可以得到的分子如图,对该分子的描述,不正确的是( )| A. | 分子式为C25H20 | |
| B. | 所有的碳原子不可能都在同一平面上 | |
| C. | 所有原子一定在同一平面上 | |
| D. | 此物质属于芳香烃类物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
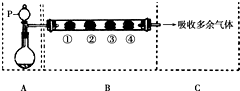 用如图装置可以完成一系列实验(图中夹持装置已略去).请回答下列问题:
用如图装置可以完成一系列实验(图中夹持装置已略去).请回答下列问题:| B中棉花的位置 | ① | ② | ③ | ④ |
| 所蘸试剂 | 石蕊试液 | 品红溶液 | 淀粉和碘 水混合液 | 氢硫酸 |
| 现象 | a | b | 褪色 | 浅黄色 |
| 体现SO2的性质 | c | d | e | f |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com