
分析 (1)首先检验装置的气密性,然后取ng样品装入广口瓶中,打开止水夹,再缓缓鼓入空气数分钟后关闭止水夹,接着在干燥管内填满碱石灰,总质量为mg,下一步缓缓加入稀硫酸至不再产生气体为止,再次打开止水夹,缓缓鼓入空气数分钟,再称干燥管总质量为wg,据此进行解答;
(2)装置中残留生成的二氧化碳,不将二氧化碳排尽,会影响测定的二氧化碳的质量,从装置中产生导出的气体中含有水,如果不除去气体中的水,会使碱石灰增重偏多,二氧化碳的质量增大;
(3)由实验目的可知,反应生成的二氧化碳的质量为(W-m)g,计算二氧化碳的物质的量,根据碳元素守恒二氧化碳的物质的量等于样品中碳酸钠的物质的量,计算样品中碳酸钠的质量,再利用质量分数的定义进行求解;
(4)装置甲中装有氢氧化钠,氢氧化钠吸收二氧化碳,可除掉空气中的二氧化碳;如果不除去气体中的二氧化碳,会使干燥管中测定的二氧化碳的质量增大;从广口瓶中产生导出的气体中含有水,如果不除去气体中的水,会使干燥管中测定的二氧化碳的质量增大.
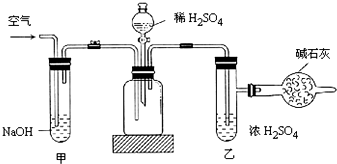
解答 解:(1)首先需要C检验装置的气密性,然后B取ng样品装入广口瓶中F打开止水夹,接着H缓缓鼓入空气数分钟,排净装置中空气,避免干扰测定结果,再E关闭止水夹,下一步A在干燥管内填满碱石灰,总质量为mg,然后G缓缓加入稀硫酸至不再产生气体为止,F打开止水夹,再次D缓缓鼓入空气数分钟,使广口瓶中的产生的二氧化碳气体全部排出,再称干燥管总质量为wg,据此可知反应生成的二氧化碳的质量为(w-m)g,所以正确的实验操作步骤为:C、B、E、H、D、A、G、E、F,
故答案为:B;H;A;E;
(2)稀硫酸和碳酸钠反应生成二氧化碳和硫酸钠和水,测定产品中Na2CO3质量分数,是通过测定稀硫酸和碳酸钠生成物中的二氧化碳的量,根据碳元素守恒,测定样品中碳酸钠质量分数,操作步骤I中,要缓缓鼓入空气数分钟,使广口瓶中的产生的二氧化碳气体全部排出;装置甲中装有氢氧化钠,氢氧化钠吸收二氧化碳,除掉空气中的二氧化碳;装置乙中装有浓硫酸,浓硫酸具有吸水性,能吸收二氧化碳中的水蒸气,
故答案为:使广口瓶中的产生的二氧化碳气体全部排出;吸收空气中的二氧化碳;吸收二氧化碳中的水蒸气;
(3)由题意可知,反应生成的二氧化碳的质量为(w-m)g,二氧化碳的物质的量n=$\frac{(w-m)g}{44g/mol}$=$\frac{w-m}{44}$mol,根据碳元素守恒可知样品中碳酸钠的物质的量n=$\frac{w-m}{44}$mol,样品中碳酸钠的质量为m=n×M=$\frac{w-m}{44}$mol×106g/mol=$\frac{53(w-n)}{22}$g,样品中碳酸钠质量分数为$\frac{\frac{53(w-n)}{22}g}{ng}$×100%=$\frac{53(w-n)}{22n}$×100%,
故答案为:$\frac{53(w-n)}{22n}$×100%;
(4)装置甲中装有氢氧化钠,氢氧化钠吸收二氧化碳,可除掉空气中的二氧化碳,鼓入空气数分钟,使广口瓶中的产生的二氧化碳气体全部排出,若去掉装置甲,空气中的二氧化碳未除去,装置中二氧化碳的质量增大,会使干燥管中测定的二氧化碳的质量增大,导致测定的样品中碳酸钠的质量增大;从广口瓶中产生导出的气体中含有水,如果不除去气体中的水,会使干燥管中测定的二氧化碳的质量增大,计算样品中碳酸钠的质量是根据碳元素守恒二氧化碳的物质的量等于样品中碳酸钠的物质的量进行计算的,所以会导致测定的样品中碳酸钠的质量增大,测定的碳酸钠质量分数偏大,
故答案为:偏大;偏大.
点评 本题考查了物质含量的测定,题目难度中等,明确实验原理、理解装置设计用途、实验目的为解答关键,注意结合相关物质的化学性质进行解,试题侧重考查学生的分析、理解能力及化学实验能力.


科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2(g)+O2(g)═2H2O(g)△H1;2H2(g)+O2(g)═2H2O(l)△H2 | |
| B. | S(g)+O2(g)═SO2(g)△H1;S(s)+O2(g)═SO2(g)△H2 | |
| C. | 2SO2(g)+O2(g)═2SO3(g)△H1;2SO3(g)═O2(g)+2SO2(g)△H2 | |
| D. | 已知反应:C(金刚石,s)═C(石墨,s)△H<0,C(金刚石,s)+O2(g)═CO2(g)△H1;C(石墨,s)+O2(g)═CO2(g)△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 这个广告有误导喜爱甜食消费者的嫌疑 | |
| B. | 糖尿病人应少吃含糖的食品,该八宝粥未加糖,可以放心食用 | |
| C. | 不加糖不等于没有糖,糖尿病人食用需慎重 | |
| D. | 不能听从厂商或广告商的宣传,应询问医生 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. ⑧的最高价氧化物的水化物的分子式H3PO4.
⑧的最高价氧化物的水化物的分子式H3PO4. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com