
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42﹣可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.下列叙述正确的是( ) 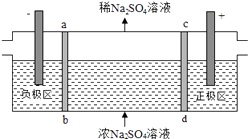
A.通电后中间隔室的SO42﹣离子向正极迁移,正极区溶液pH增大
B.该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C.负极反应为2H2O﹣4e﹣=O2+4H+ , 负极区溶液pH降低
D.当电路中通过1mol电子的电量时,会有0.5mol的O2生成
【答案】B
【解析】解:A、阴离子向阳极(即正极区)移动,氢氧根离子放电pH减小,故A错误;B、直流电场的作用下,两膜中间的Na+和SO42﹣可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室,通电时,氢氧根离子在阳极区放电生成水和氧气,考虑电荷守恒,两膜中间的硫酸根离子会进入正极区,与氢离子结合成硫酸;氢离子在阴极得电子生成氢气,考虑电荷守恒,两膜中间的钠离子会进入负极区,与氢氧根离子结合成氢氧化钠,故可以得到NaOH和H2SO4产品,故B正确;
C、负极即为阴极,发生还原反应,氢离子得电子生成氢气,故C错误;
D、每生成1mol氧气转移4mol电子,当电路中通过1mol电子的电量时,会有0.25mol的O2生成,故D错误.
故选B.
A、阴离子向阳极(即正极区)移动,氢氧根离子放电pH减小;
B、从两极的电极反应和溶液的电中性角度考虑;
C、负极即为阴极,发生还原反应,氢离子放电;
D、当电路中通过1mol电子的电量时,会有0.25mol的O2生成.


科目:高中化学 来源: 题型:
【题目】关于药品的取用,下列说法不正确的是( )
①实验中剩余的药品要放回原试剂瓶,以免浪费
②实验中剩余的药品应该扔掉
③实验中剩余的药品要倒入废液缸中
④剩余的固体药品应放回原试剂瓶,液体应倒入废液缸中
A. ① B. ② C. ②③ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,22.4LHCl气体溶于50mL水再配成250mL溶液,求:
(1)所得盐酸的物质的量浓度为;
(2)若将此溶液再稀释成1L溶液,则稀释后盐酸的物质的量浓度变为;
(3)将(2)的溶液取出250mL与足量Zn反应可以产生的H2在标准状况下的体积为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在同温、同压条件下,两种物质的量相同的单质气体之间的关系 ( )
①体积都是22.4 L ②具有相同的体积
③都是双原子分子 ④具有相同的分子数目
A. ①③ B. ②④
C. ①④ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,向一密闭容器中充入2 mol SO2和2 mol O2 , 在一定条件下发生反应:2SO2+O2 ![]() 2SO3 , 该反应达到最大限度时,下列说法正确的是( )
2SO3 , 该反应达到最大限度时,下列说法正确的是( )
A.正反应的速率为零
B.SO2完全转化为SO3
C.SO3的物质的量浓度不再变化
D.SO2、O2和SO3的物质的量浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是部分短周期中第二、第三周期元素的原子半径及主要化合价。
元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
原子半径(nm) | 0.186 | 0.160 | 0.152 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
主要化合价 | +1 | +2 | +1 | +3 | +5、-3 | +7、-1 | +5、-3 | -2 |
回答下列问题:
(1)⑧在元素周期表中的位置是(周期、族);
(2)8个元素的最高价氧化物的水化物中,酸性最强的是(填化学式);
(3)元素⑤、⑦、⑧分别形成的简单气态氢化物中,⑦的电子式为 , 稳定性最强的氢化物的结构式为;
(4)写出①、④的最高价氧化物对应的水化物之间发生反应的离子方程式;
(5)用电子式表示元素①与⑥形成化合物的过程。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香樟树中可提取一种有机物樟脑(键线式如图  ),下列有关说法正确的是( )
),下列有关说法正确的是( )
A.樟脑的分子式为C10H18O
B.樟脑中含有2种官能团
C.樟脑在一定条件下可以发生消去反应
D.樟脑有一种特殊的气味,但不属于芳香烃类物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如下图所示。下列说法正确的是 ( )
A.苛性钾溶液中KOH的质量是5.6 g
B.反应中转移电子的物质的量是0.18mol
C.在酸性条件下 ClO-和ClO3-可生成Cl2
D.一定有3.136 L氯气参与反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】瑞典ASES公司设计的曾用于驱动潜艇的液氨﹣液氧燃料电池示意图如图所示,下列有关说法正确的是( ) 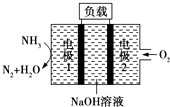
A.电池工作时,Na+向电极1移动
B.电池工作一段时间后停止,溶液PH值比开始时明显减小
C.电极1发生的电极反应为2NH3+6OH﹣﹣6e﹣═N2↑+6H2O
D.用该电池做电源电解精炼铜,理论上每消耗0.2 mol NH3的同时阳极会得到19.2g纯铜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com