
 ��
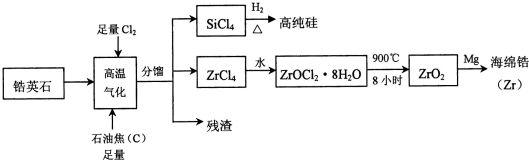
������ �Ӣʯ����Ҫ�ɷ�ΪZrSiO4��Ҳ�ɱ�ʾΪZrO2•SiO2����������Al2O3��SiO2��Fe2O3�����ʣ���ͨ�������������Լ���������ʯ���ͷ�Ӧ��ZrSiO4ת��ΪZrCl4����ˮˮ�⣬ʹZrCl4ת��ΪZrOCl2•8H2O��900����ȷֽ⣬���ɵõ�ZrO2������þ�û��õ�����ﯣ�����þ�û��õ�����ﯣ�
��1�������ڻ��������������ϼ۴�����Ϊ�㣬���ZrSiO4�Ļ�ѧʽ���н��SiCl4�����й�ԭ���������4�����ӣ����γ�4�����ۼ��ﵽ�ȶ��ṹ��ÿ����ԭ�����γ�һ�����ۼ��ﵽ�ȶ��ṹ��
��2�����Ӣʯ��������SiO2��SiO2Ҳ���ڸ������������·�Ӧ����SiCl4��
��3������̼���������Ļ�ѧ���ʵIJ�����з��룬������Ϊ���������
��4������ͼʾZrCl4��ˮ��Ӧ����ΪZrOCl2•8H2O�����ԭ���غ���н��
��5��ȼ�����ڼ�Ϊ����������ʧȥ���ӷ���������Ӧ��Ϊ��ϩʧ���Ӻ������ӷ�Ӧ���ɶ�����̼��ˮ��4.44g Cu2��OH��2CO3�����ʵ���Ϊ0.02mol������0.02molCu2��OH��2CO3ʹ��Һ��ԭ���൱������ͭ��Һ�ڵ������в�����0.4moCu��������0.2molˮ���ݴ˼������ת�Ƶ����ʵ�����
��� �⣺�Ӣʯ����Ҫ�ɷ�ΪZrSiO4��Ҳ�ɱ�ʾΪZrO2•SiO2����������Al2O3��SiO2��Fe2O3�����ʣ���ͨ�������������Լ���������ʯ���ͷ�Ӧ��ZrSiO4ת��ΪZrCl4����ˮˮ�⣬ʹZrCl4ת��ΪZrOCl2•8H2O��900����ȷֽ⣬���ɵõ�ZrO2������þ�û��õ�����ﯣ�����þ�û��õ�����ﯣ�
��1�������ڻ��������������ϼ۴�����Ϊ�㣬��Ԫ����-2�ۣ���Ԫ����+4�ۣ����Ԫ�أ�Zr���Ļ��ϼ���x����֪ZrSiO4���Ԫ�أ�Zr���Ļ��ϼۣ�x+��+4��+��-2����4=0����x=+4��SiCl4�����й�ԭ���������4�����ӣ����γ�4�����ۼ��ﵽ�ȶ��ṹ��ÿ����ԭ�����γ�һ�����ۼ��ﵽ�ȶ��ṹ������ʽΪ�� ��
��
�ʴ�Ϊ��+4�� ��
��
��2���Ӣʯ����Ҫ�ɷ�ΪZrSiO4��Ҳ�ɱ�ʾΪZrO2•SiO2����������Al2O3��SiO2��Fe2O3�����ʣ�������SiO2Ҳ���ڸ������������·�Ӧ����SiCl4��������õ���SiCl4����ͨ�����ɴ�ZrSiO4�����ķ�Ӧ�õ���SiCl4������
�ʴ�Ϊ����Ϊ�����е�SiO2Ҳͨ����Ӧ������SiCl4��
��3��������Ϊ���������������ǿ��ǿ�̼�����ڷ��������ᣬ�����ڼ�������з����C��A12O3���ֹ��壺�Ӽ��ȡ���˵õ�C��������Һ��ͨ������CO2�����˺�����ȵõ�����������������ȡ���˵õ�C��������Һ�мӰ�ˮ�����˺�����ȵõ�����������
�ʴ�Ϊ���Ӽ��ȡ���˵õ�C��������Һ��ͨ������CO2�����˺�����ȵõ�����������������ȡ���˵õ�C��������Һ�мӰ�ˮ�����˺�����ȵõ�����������
��4��ZrCl4��ˮ��Ӧ����ΪZrOCl2•8H2O������ԭ���غ㣬��Ӧ����ʽΪ��ZrCl4+9H2O�TZrOCl2•8H2O+2HCl��
�ʴ�Ϊ��ZrCl4+9H2O�TZrOCl2•8H2O+2HCl��
��5����ȼ�ϵ����ͨ����ϩ��һ��Ϊ����������������Ӧ����ϩʧ���Ӻ������ӷ�Ӧ���ɶ�����̼��ˮ���缫��ӦʽΪ��C2H4+6O2--12e-�T2CO2+2H2O��4.44g Cu2��OH��2CO3�����ʵ���Ϊ0.02mol������0.02molCu2��OH��2CO3ʹ��Һ��ԭ���൱������ͭ��Һ�ڵ������в�����0.04moCu��������0.02molˮ�����ݹ�ϵʽCu��2e-��֪��������0.04moCuҪת��0.08mol���ӣ����ݹ�ϵʽH2O��2e-����֪������0.02molˮ��ת�Ƶ��ӵ����ʵ���Ϊ0.04mol�����Է�Ӧ�й�ת�Ƶ��ӵ����ʵ���Ϊ0.12mol��
�ʴ�Ϊ��C2H4+6O2--12e-�T2CO2+2H2O��0.12mol��
���� ���⿼���˺���ﯵ��Ʊ��Լ����ʷ����ᴿ�ķ��������̷���Ӧ�ã��漰���̵ķ���Ӧ�á����ӷ���ʽ����д������ʵ����������ԭ����Ӧ�ü�����ȣ�������ѧ���ķ���������ʵ�������Ŀ��飬��������Ŀ��ע�����ʵ��ԭ���Ͳ������̵�Ŀ�ģ���Ҫ���������ʵ����⣬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | ���� |
| ��ʢ��4gNa2O2���ձ��м���50mL����ˮ�õ���Һa | ���з�Ӧ��������ʹ������ľ����ȼ������ |
| ȡ5mL��Һa���Թ��У��������η�̪ | ������Һ��� ����10���ֺ���Һ��ɫ���Ա�dz���Ժ���Һ��Ϊ��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
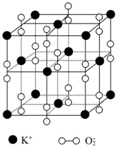 ��ͼ��ʾ�Ǽء�����Ԫ���γɵ�һ�־����һ����������������С���ظ���Ԫ�������������Ļ��ϼۿɿ����Dz���Ϊ0�ۣ�����Ϊ-2�ۣ�
��ͼ��ʾ�Ǽء�����Ԫ���γɵ�һ�־����һ����������������С���ظ���Ԫ�������������Ļ��ϼۿɿ����Dz���Ϊ0�ۣ�����Ϊ-2�ۣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
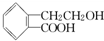 ������ͨ����ͬ��ѧ��Ӧ�ֱ��Ƶ�B��C��D�������ʣ�
������ͨ����ͬ��ѧ��Ӧ�ֱ��Ƶ�B��C��D�������ʣ�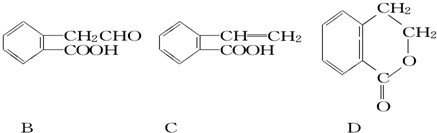
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
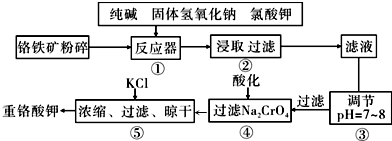
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
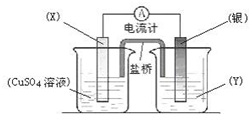 ����������ԭ��Ӧ��2Ag+��aq��+Cu��s���TCu2+��aq��+2Ag��s����Ƶ�ԭ�����ͼ��ʾ��
����������ԭ��Ӧ��2Ag+��aq��+Cu��s���TCu2+��aq��+2Ag��s����Ƶ�ԭ�����ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͨ��CH4�ĵ缫Ϊ���� | |
| B�� | �����ĵ缫��ӦʽΪO2+4H++4e-�T2H2O | |
| C�� | ͨ��CH4��һ���ĵ缫��ӦʽΪCH4+2O2+4e-�TCO2+2H2O | |
| D�� | �����ĵ缫��ӦʽΪCH4+10OH--8e-�TCO32-+7H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ����������ԭ��Ӧ2Ag+��aq��+Cu��s���TCu2+��aq��+2Ag��s����Ƶ�ԭ�����ͼ��ʾ��
����������ԭ��Ӧ2Ag+��aq��+Cu��s���TCu2+��aq��+2Ag��s����Ƶ�ԭ�����ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
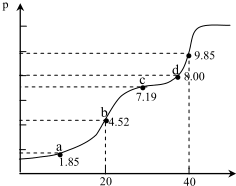
| A�� | a ��������Һ�У�2n��H2A��+n��A2-��=0.002mol | |
| B�� | b ��������Һ�У�c��H2A��+c��H+��=c��A2-��+c��OH-�� | |
| C�� | c ��������Һ�У�c��Na+����3c��HA-�� | |
| D�� | d ��������Һ�У�c��Na+����c��A2-����c��HA-�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com