
 ����β����ȼúβ��������ҳ�����Ⱦ������ɿ�����Ⱦ����Ҫԭ��
����β����ȼúβ��������ҳ�����Ⱦ������ɿ�����Ⱦ����Ҫԭ��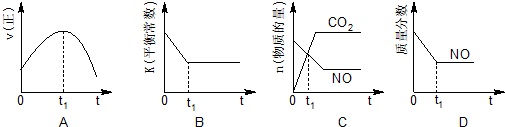
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ�� ����ʱ��/min | ||
| CO2��g�� | H2��g�� | H2O��g�� | CO2��g�� | |||
| 1 | 650 | 2 | 1 | 0.4 | 1.6 | 6 |
| 2 | 900 | 4 | 2 | 1.6 | 2.4 | 2 |
���� ��1���ٸ��ݵ���ƽ���ʱ���ж��¶ȸߵͣ�����ƽ��ʱ������̼��Ũ���ж��¶ȶ�ƽ���Ӱ�죻
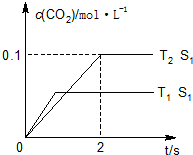
����ͼ��֪��T2�¶�ƽ��ʱ��������̼��Ũ�ȱ仯��Ϊ0.1mol/L������v=$\frac{��c}{t}$����v��CO2�����ٸ�������֮�ȵ��ڻ�ѧ������֮�ȼ���v��N2����
�۽Ӵ����Խ��Ӧ����Խ�죬����ƽ���ʱ��Խ�̣������ı����S1��S2��S2�����´ﵽƽ������ʱ���������������Ӱ��ƽ���ƶ���ƽ��ʱ������̼��Ũ�����¶�T1����ƽ��ʱ��ͬ��
��A������ƽ���������������ȣ����ٱ仯��
B������ƽ����¶�Ϊ��ֵ��ƽ�ⳣ�����䣬��Ϸ�Ӧ���ж��淴Ӧ�����������¶ȱ仯���ж��¶ȶԻ�ѧƽ�ⳣ����Ӱ�죻
C��t1ʱ�̺������̼��NO�����ʵ��������仯������ٱ仯��
D������ƽ������ֵĺ����������仯��
��2�����ݸ�˹���ɣ�����֪�Ȼ�ѧ����ʽ�����ʵ���ϵ�����мӼ�����Ŀ���Ȼ�ѧ����ʽ��
��3������������ʽ����ƽ��ʱ������ֵ����ʵ������÷�Ӧ�������������ķ�Ӧ�����������ʵ�������Ũ�ȴ���ƽ�ⳣ������ʽ����ƽ�ⳣ����
�ڵڶ����¶ȱȵ�һ��ߣ���Ӧ�����ʵ����ȵ�һ������һ����ƽ��ʱCO2�����ʵ����ȵ�һ��Ķ࣬�����÷�ӦΪ���ȷ�Ӧ��
��� �⣺��1������ͼ1��֪���¶�T1�ȵ���ƽ�⣬���¶�T1��T2���¶�Խ��ƽ��ʱ��������̼��Ũ��Խ�ͣ�˵�������¶�ƽ�����淴Ӧ�ƶ���������ӦΪ���ȷ�Ӧ��
�ʴ�Ϊ������
����ͼ��֪��T2�¶�ʱ2s����ƽ�⣬ƽ��ʱ������̼��Ũ�ȱ仯��Ϊ0.1mol/L����v��CO2��=$\frac{0.1mol/L}{2s}$0.05mol/��L•s��������֮�ȵ��ڻ�ѧ������֮�ȣ���v��N2��=0.5v��CO2��=0.5��0.05mol/��L•s��=0.025mol/��L•s����
�ʴ�Ϊ��0.025mol/��L•s����
�۽Ӵ����Խ��Ӧ����Խ�죬����ƽ���ʱ��Խ�̣������ı����S1��S2��S2�����´ﵽƽ������ʱ���������������Ӱ��ƽ���ƶ���ƽ��ʱ������̼��Ũ�����¶�T1����ƽ��ʱ��ͬ����c��CO2����T1��S2�����´ﵽƽ������еı仯����Ϊ�� ��
��
�ʴ�Ϊ�� ��
��
��A������ƽ���������������ȣ����ٱ仯��t1ʱ��V�����֮���淴Ӧ�������ʷ����仯��δ����ƽ�⣬��A����
B���÷�Ӧ����ӦΪ���ȷ�Ӧ���淴Ӧ�����¶����ߣ���ѧƽ�ⳣ����С������ƽ����¶�Ϊ��ֵ������ߣ�ƽ�ⳣ�����䣬��B��ȷ��
C��t1ʱ�̺������̼��NO�����ʵ��������仯��t1ʱ��δ����ƽ��״̬����C����
D��NO����������Ϊ��ֵ��t1ʱ�̴���ƽ��״̬����D��ȷ��
�ʴ�Ϊ��BD��
��2����֪��CH4��g��+2NO2��g���TN2��g��+CO2��g��+2H2O��g����H1=-867kJ/mol��
2NO2��g��?N2O4��g����H2=-56.9kJ/mol��
H2O��g��=H2O��l����H=-44.0kJ/mol��
���ݸ�˹���ɣ���-��+�ܡ�2�ɵ�CH4��g��+N2O4��g��=N2��g��+CO2��g��+2H2O��l�����ʡ�H=-867kJ/mol-��-56.9kJ/mol��+2��-44.0��kJ/mol=-898.1kJ/mol ��CH4��g��+N2O4��g���TN2��g��+2H2O��l��+CO2��g����H=-898.1kJ/mol��
�ʴ�Ϊ��CH4��g��+N2O4��g���TN2��g��+2H2O��l��+CO2��g����H=-898.1kJ/mol��
��3����ƽ��ʱCO2�����ʵ���Ϊ1.6mol����
CO��g��+H2O��g��?CO2��g��+H2��g����
��ʼ��mol����2 1 0 0
�仯��mol����0.6 0.6 1.6 1.6
ƽ�⣨mol����1.4 0.4 1.6 1.6
�÷�Ӧǰ������������䣬���������ʵ�������Ũ�ȼ���ƽ�ⳣ������650��ʱ�÷�Ӧƽ�ⳣ��k=$\frac{1.6��1.6}{1.4��0.4}$=4.57��
�ʴ�Ϊ��4.57��
��ʵ��1��CO2��ת����Ϊ$\frac{2-1.6}{2}$��100%=20%��ʵ��2��CO2��ת����Ϊ$\frac{4-2.4}{4}$��100%=40%����ʵ��1��ת����С��ʵ��2����˵���¶�����ƽ��������Ӧ�����ƶ�������Ӧ���ȣ��ʴ�Ϊ������
���� ���⿼�黯ѧƽ��ͼ��ѧ��Ӧ���ʡ�Ӱ�컯ѧƽ������ء�ƽ�ⳣ������ȣ���Ŀ�ۺ��Խϴ��ѣ��Ƕ�֪ʶ���ۺ����á�ע�����֪ʶ���������գ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
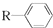 $��_{һ������}^{CO��HCl}$
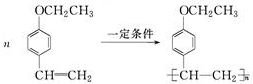
$��_{һ������}^{CO��HCl}$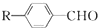 ��Ϊ�ϳ�ij��Һ�����ϵ��м���M������������²�ͬ�ĺϳ�;����
��Ϊ�ϳ�ij��Һ�����ϵ��м���M������������²�ͬ�ĺϳ�;����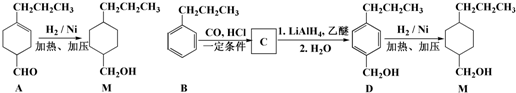
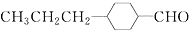 ��
��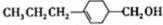 ��д�ṹ��ʽ�����ɣ�
��д�ṹ��ʽ�����ɣ�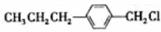 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
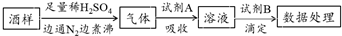
| A�� | ���Ѿ��м��������ε���ҪĿ���Ƿ�ֹ�������������������εĻ�ԭ�� | |
| B�� | ͨ��N2����е�Ŀ����Ϊ�˽��������������Һ��ȫ���ϳ� | |
| C�� | ���Լ�Aѡ����ˮ�����Լ�B��ѡ��NaOH��Һ | |
| D�� | ���Լ�Aѡ���Һ���������պ���ҺΪ���ԣ����Լ�B��ѡ��I2��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  | B�� |  | C�� |  | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
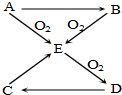 ��֪A��B��C��D��E������������ͼ��ʾ��ת����ϵ�����ַ�Ӧ�P��Ӧ����δ�г���������ʱ��Ҫ�������������裩�������������о�����AԪ�أ�
��֪A��B��C��D��E������������ͼ��ʾ��ת����ϵ�����ַ�Ӧ�P��Ӧ����δ�г���������ʱ��Ҫ�������������裩�������������о�����AԪ�أ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH3OCH3 | B�� | CH3CH2OH | C�� | CH3CH2CH3 | D�� | CH3COCH2CH3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ �� �� �� | ʵ �� �� �� |
| ��1����9.0g A��������O2�г��ȼ�գ���ʹ��������λ���ͨ��������Ũ����ͼ�ʯ�ң��������߷ֱ�����5.4g��13.2g�� | ��1��A��ʵ��ʽΪCH2O�� |
| ��2��ͨ�������������Է�������Ϊ90�� | ��2��A�ķ���ʽΪC3H6O3�� |
| ��3����ȡ9.0g A����������NaHCO3��ĩ��Ӧ������2.24L CO2����״�������������������Ʒ�Ӧ������2.24L H2����״������ | ��3��A�к��еĹ���������Ϊ�Ȼ����ǻ��� |
| ��4��A�ĺ˴Ź����������������շ壬������֮��Ϊ2��2��1��1�� | ��4������������A�Ľṹ��ʽΪ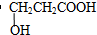 �� ����5��д��A��NaHCO3��Ӧ�Ļ�ѧ����ʽ 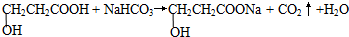 �� �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӱ뾶��Na��Cl | B�� | ���ȶ��ԣ�HCI��HF | ||
| C�� | ���Ӱ뾶��F-��Mg2+ | D�� | ���ԣ�NaOH��Mg��OH��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
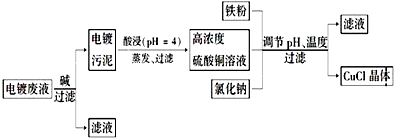
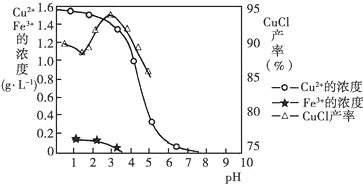
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com