
| A. | 有10NA个电子转移时,放出1300kJ的能量 | |
| B. | 有1NA个水分子生成且为液体时,吸收1300kJ的能量 | |
| C. | 有2NA个碳氧共用电子对生成时,放出1300kJ的能量 | |
| D. | 有8NA个碳氧共用电子对生成时,吸收1300kJ的能量 |
分析 A、此反应转移10 mol电子,放出1 300 kJ能量;
B、该反应为放热反应;
C、1 mol CO2分子中含有4 mol碳氧共用电子对,有8NA个碳氧共用电子对生成时,即生成了2 mol CO2,放出1 300 kJ的能量;
D、1 mol CO2分子中含有4 mol碳氧共用电子对,有8NA个碳氧共用电子对生成时,即生成了2 mol CO2,放出1 300 kJ的能量.
解答 解:A、反应中每当有1 mol C2H2参加反应,转移10 mol电子,放出1 300 kJ能量,故A正确;
B、由热化学方程式看出,△H=-1300kJ/mol,故该反应为放热反应,故B错误;
C、由于1 mol CO2分子中含有4 mol碳氧共用电子对,故此反应中有8NA个碳氧共用电子对生成,放出1 300 kJ的能量,则当有2NA个碳氧共用电子对生成时,放出$\frac{1300KJ}{4}$=325KJ的能量,则故C错误;
D、1 mol CO2分子中含有4 mol碳氧共用电子对,故此反应中有8NA个碳氧共用电子对生成,放出1 300 kJ的能量,而不是吸收,故D错误.
故选A.
点评 本题考查了热化学方程式计算应用,主要是电子转移和化学键形成与反应热量的定量计算应用,掌握基础是关键,题目难度中等.


 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案科目:高中化学 来源: 题型:推断题
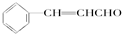 )在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如图路线合成的:
)在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如图路线合成的: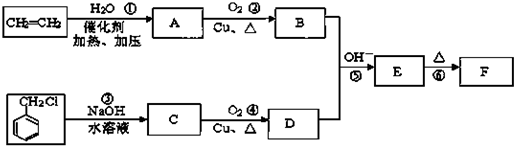
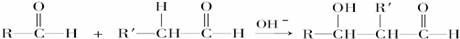
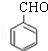 ;
;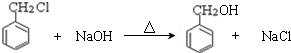 ,判断有关反应的类型:⑥消去反应;
,判断有关反应的类型:⑥消去反应;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 次氯酸的结构式:H-Cl-O | B. | CO2的比例模型  | ||
| C. | 甲基的电子式: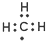 | D. | 硬脂酸的化学式:C17H33COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | Ka=1.8×10-5 | Kal=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
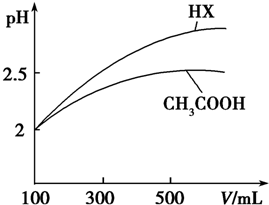
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸、水煤气、醋酸、干冰 | B. | 液氯、氯水、硫酸钠、乙醇 | ||
| C. | 空气、天然气、苛性钾、硫酸钡 | D. | 胆矾、漂白粉、氯化钾、氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图所示,一悬挂的铜球浸没在稀硫酸溶液中,且铜球不与烧杯接触,现往稀硫酸中投入一铁片,待铁片充分反应后,铜球所受的拉力变化情况是( )
如图所示,一悬挂的铜球浸没在稀硫酸溶液中,且铜球不与烧杯接触,现往稀硫酸中投入一铁片,待铁片充分反应后,铜球所受的拉力变化情况是( )| A. | 变大 | B. | 变小 | C. | 不变 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com