
某温度下,向一定体积0.1 mol/L的氨水中逐滴滴加0.1mol/L的盐酸,溶液中pH与pOH[注:pOH=-lgc(OH-)]的变化关系如图所示,则下列说法中错误的是

A.M点所示溶液中c( NH4+)>c(Cl-)
B.Q点所示溶液的导电熊力强于M点
C.Q点消耗盐酸的体积等于氨水的体积
D.M点和N点所示溶液中水的电离程度相同
C
【解析】
试题分析:A、M点的pH值大于pOH值,所以溶液中氢离子浓度小于OH-浓度,即溶液显碱性。所以根据电荷守恒c( NH4+)+c(H+)=c(Cl-)+c(OH-)可知,M点所示溶液中c( NH4+)>c(Cl-),A正确;B、Q点所示溶液中pH值等于pOH值,说明溶液显中性。由于向一定体积0.1 mol/L的氨水中逐滴滴加0.1mol/L的盐酸时,溶液的酸碱性变化为碱性→中性→酸性,而氨水是弱碱,因此Q点的导电熊力强于M点,B正确;C、氨水与盐恰好反应时,生成的NH4+水解溶液显酸性。而Q点显中性,说明氨水过量,所以Q点消耗盐酸的体积小于氨水的体积,C不正确;D、M点氨水过量,N点盐酸过量,且N点溶液中氢离子浓度与M点溶液中OH-浓度相等,所以M点和N点所示溶液中水的电离程度相同,D正确,答案选C。
考点:考查酸碱中和反应、溶液中离子浓度比较、溶液导电性、酸碱性以及外界条件对水电离平衡的影响


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
 某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=-lg[OH-])与pH的变化关系如图所示,则( )
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=-lg[OH-])与pH的变化关系如图所示,则( )| A、M点所示溶液导电能力强于Q点 | B、N点所示溶液中c(CH3COO-)>c(Na+) | C、M点和N点所示溶液中水的电离程度相同 | D、Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:
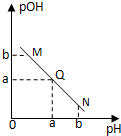 某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH( pOH=-lgc(OH-))与pH的变化关系如图所示,则( )
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH( pOH=-lgc(OH-))与pH的变化关系如图所示,则( )| A、N点所示溶液中c(H+)<c(OH-) | B、M点所示溶液导电能力强于Q点 | C、M点水的电离程度大于N点 | D、Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中
pOH(pOH=-lg[OH-])与pH的变化关系如图所示,则
A.M点所示溶液导电能力强于Q点
B.N点所示溶液中c(CH3COO-)﹥c(Na+)
C.M点和N点所示溶液中水的电离程度相同
D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积

查看答案和解析>>
科目:高中化学 来源:2013-2014学年四川省成都市高三第一次诊断考试理综化学试卷(解析版) 题型:选择题
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=-lg[OH-])与pH的变化关系如图所示,则( )

A.M点所示溶液导电能力强于Q点
B.N点所示溶液中c(CH3COO-)>c(Na+)
C.M点和N点所示溶液中水的电离程度相同
D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com