
下列各组物质的无色溶液,不用其它试剂即可鉴别的是 ( )
①KOH Na2SO4 AlCl3 ②NaHCO3 Ba(OH)2 H2SO4
③HCl NaAlO2 NaHSO4 ④Ca(OH)2 Na2CO3 BaCl2
A.①② B.②③ C.①③④ D.①②④
科目:高中化学 来源: 题型:
用化学术语回答下列问题:
(1)由氢气和氧气反应生成1 mol水蒸气放热241.8 kJ·mol-1,写出其热化学方程式: .
若1g水蒸气转化成液态水放热2.444kJ,则反应H2(g)+1/2 O2(g)==H2O(l)
的△H= kJ·mol-1,氢气的燃烧热为 kJ·mol-1。
(2)电解硝酸银溶液电极反应式(惰性电极)
①阳极:
②阴极:
(3)银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示为:
2Ag+Zn(OH)2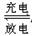 Ag2O+Zn+H2O在此电池放电时,正极的电极反应式为 。
Ag2O+Zn+H2O在此电池放电时,正极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对化学反应的认识正确的是( )
A.在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向
B.如果某化学反应的ΔH和ΔS均小于0,则反应一定能自发进行
C.化学反应过程中,一定有化学键的断裂和形成
D.反应物的总焓大于生成物的总焓时,ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.KClO3 和SO3 溶于水后能导电,故KClO3 和SO3 为电解质
B.25℃时、用醋酸溶液滴定等浓度NaOH 溶液至pH=7,V 醋酸<V NaOH
C.向NaAlO2 溶液中滴加NaHCO3 溶液,有沉淀和气体生成
D.AgCl 易转化为AgI 沉淀且K(AgX)=c(Ag+ )·c(X—),故K(AgI)<K(AgCl)
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列各溶液中,离子一定能大量共存的是 ( )
A.强碱性溶液中:K+、Al3+、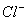 、
、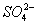
B.含有0.1 mol·L-1 Fe3+的溶液中:K+、Mg2+、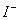 、
、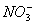
C.含有0.1 mol·L-1Ca2+溶液在中:Na+、K+、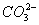 、
、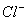
D.室温下,pH=1的溶液中: Na+、Fe3+、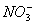 、
、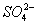
查看答案和解析>>
科目:高中化学 来源: 题型:
用物质的量都是0.1 mol的CH3COOH和CH3COONa配制成1L混合溶液,已知其中
C(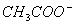 )>C(Na+),对该混合溶液的下列判断正确的是 ( )
)>C(Na+),对该混合溶液的下列判断正确的是 ( )
A.C(H+)>C(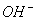 )
)
B.C(CH3COOH)+C(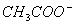 )=0.2 mol/L
)=0.2 mol/L
C.C(CH3COOH)>C(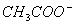 )
)
D.C(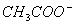 )+C(OH-)=0.2 mol/L
)+C(OH-)=0.2 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在溶液中不能大量共存,且加入过量NaOH溶液或过量稀盐酸均能得到澄清溶液的是 ( )
A. Fe3+、CI-、Na+、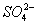 B. Al3+、Na+、
B. Al3+、Na+、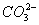 、
、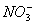
C. Ag+、Na+、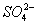 、
、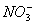 D. AlO2-、
D. AlO2-、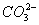 、K+、Na+
、K+、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
以下是25℃时几种难溶电解质的溶解度:
| 难溶电解质 | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 溶解度/g | 9×12-4 | 1.7×12-6 | 1.5×12-4 | 3.0×12-9 |
在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些离子。例如:
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,加入一定量的试剂反应,过滤结晶
② 为了除去氯化镁晶体中的杂质Fe3+,先将混合物溶于水,加入足量的氢氧化镁,充分反应,过滤结晶
③ 为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶
请回答下列问题:
(1)上述三个除杂方案都能够达到很好效果,Fe2+、Fe3+都被转化为 而除去
(2)①中加入的试剂应该选择_________为宜,其原因是________________________。
(3)②中除去Fe3+所发生的总反应的离子方程式为_____________________________。
(4)下列与方案③相关的叙述中,正确的是__________________(填字母)。
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.调节溶液pH=4可选择的试剂是氢氧化铜或碱式碳酸铜
D.Cu2+可以大量存在于pH=4的溶液中
E.在pH>4的溶液中Fe3+一定不能大量存在
查看答案和解析>>
科目:高中化学 来源: 题型:
在冶金工业上,通常均不能用化学还原剂制得的金属组是( )
A.Na、Ba、Mg、A1 B.Zn、Fe、Cu、Ag
C.Na、K、Zn、Fe D.Mg、Al、Zn、Fe
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com