
【题目】已知温度T时水的离子积常数为Kw,该温度下,将浓度为amol/L的一元酸HA与bmol/L的一元碱BOH等体积混合,可判断该溶液呈中性的依据是:
A. a=b
B. 混合溶液的pH值为7
C. 混合溶液中C(H+)=![]()
D. 混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
科目:高中化学 来源: 题型:
【题目】【江西省景德镇市2017届高三第二次模拟理综化学试题】(1)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)![]() CO2(g)+H2(g);△H<0。CO和H2O浓度变化如图,则04 min的平均反应速率v(CO)=______________ mol/(L·min)
CO2(g)+H2(g);△H<0。CO和H2O浓度变化如图,则04 min的平均反应速率v(CO)=______________ mol/(L·min)
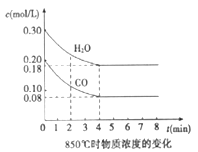
(2)t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表。
时间(min) | CO | H2O | CO2 | H2 |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | c1 | c2 | c3 | c4 |
4 | c1 | c2 | c3 | c4 |
5 | 0.116 | 0.216 | 0.084 | |
6 | 0.096 | 0.266 | 0.104 |
请回答:
①表中34 min之间反应处于_____________状态;c3数值_____________0.12 mol/L(填大于、小于或等于)。
②反应在45 min间,平衡向逆方向移动,可能的原因是_____________(单选),表中56 min之间数值发生变化,可能的原因是_____________(单选)。
a.增加了水蒸气的量 b.升高温度 c.使用催化剂 d.增加压强
(3)如图是一个电化学的装置图。
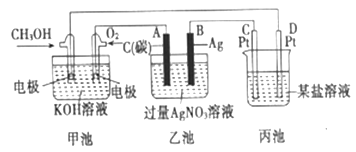
①图中乙池是________装置(填“电解池”或“原电池”)甲池中OH-移向____________极(填“CH3OH”或“O2”)。若丙池中为400ml 1mol/L硫酸铜溶液,当外电路有1mol电子通过时,C、D两极共产生_______mol的气体。
②写出B电极的电极反应式:_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电化学的叙述中,不正确的是( )
A.原电池中,电极材料不一定参加反应
B.电解池中,阴极上得到电子的物质不一定是电解质提供的阳离子
C.原电池工作时,溶液中的阴离子向负极移动
D.原电池中,电子从负极经外电路流向正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同浓度的下列溶液:①NH4HSO4 ②(NH4)2SO4③(NH4)2Fe(SO4)2 ④NH4HCO3 ⑤NH3·H2O,其中NH4+的浓度的由大到小顺序为
A. ②③④①⑤ B. ③②⑤①④ C. ③②①④⑤ D. ⑤③②①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 物质的量就是物质的数量 B. 物质的量是国际单位制中基本物理量之一
C. 阿伏加德罗常数就是6.02×1023mol-1 D. 物质的量的单位——摩尔只适用于分子、原子、离子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com