
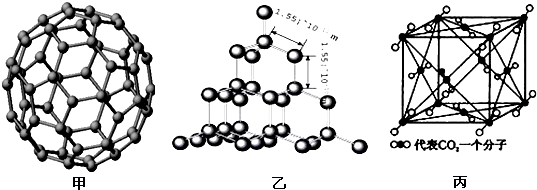
下面是C60、金刚石和二氧化碳的分子模型。
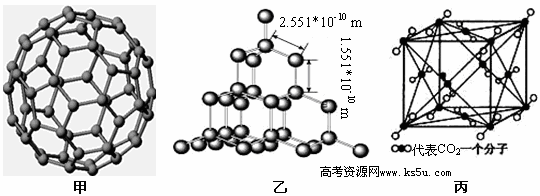
请回答下列问题:
(1)硅与碳同主族,写出硅原子基态时的核外电子排布式:_________________
(2)从晶体类型来看,C60属于_________晶体。
(3)二氧化硅结构跟金刚石结构相似,即二氧化硅的结构相当于在硅晶体结构中每个硅与硅的化学键之间插入一个O原子。观察图乙中金刚石的结构,分析二氧化硅的空间网状结构中,Si、O原子形成的最小环上O原子的数目是__________________________;晶体硅中硅原子与共价键的个数比为
(4)图丙是二氧化碳的晶胞模型,图中显示出的二氧化碳分子数为14个。实际上一个二氧化碳晶胞中含有________个二氧化碳分子,二氧化碳分子中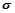 键与
键与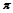 键的个数比为
。
键的个数比为
。
(5)有机化合物中碳原子的成键方式有多种,这也是有机化合物种类繁多的原因之一。丙烷分子中2号碳原子的杂化方式是_______,丙烯分子中2号碳原子的杂化方式是_______,丙烯分子中最多有 个原子共平面。
(1)1s22s22p63s23p2 (2)分子 (3)6 ;1:2 (4)4 ;1:1(5)sp3 ;sp2 ;7
【解析】
试题分析:(1)硅的原子数序为14,基态时的核外电子排布式为1s22s22p63s23p2;(2)由题给结构模型知,C60有固定的组成,不属于空间网状结构,为分子晶体;(3)由题给结构模型知,金刚石中的最小环为六元环,二氧化硅结构跟金刚石结构相似,Si、O原子形成的最小环上应有6个Si原子,硅晶体结构中每个硅与硅的化学键之间插入一个O原子,则Si、O原子形成的最小环上O原子的数目是6,二氧化硅晶体中,每个Si原子与4个O原子形成共价键,每一个共价键中Si的贡献为一半,则平均1个Si原子形成2个共价键,所以晶体硅中硅原子与共价键的个数比为1:2;(4)二氧化碳的晶胞中,二氧化碳分子位于晶胞的顶点和面心位置,则晶胞中含有二氧化碳的分子数为8×1/8+6×1/2=4,二氧化碳的分子结构为O=C=C,每个分子中含有2个σ键和2个π键,所以σ键与π键的个数比为1:1;(5)根据丙烷和丙烯的结构分析,丙烷分子中2号碳原子形成4个σ键,所以杂化方式是sp3,丙烯分子中2号碳原子碳原子形成3个σ键,所以杂化方式是sp2,丙烯中含有乙烯的结构特点,和双键共平面的原子共有6个原子,甲基中含C-H键,原子围绕着σ键旋转,则最多有1个原子和其它6个原子共平面,即丙烯分子中最多有7个原子共平面。
考点:考查电子排布式的书写、晶胞的结构、杂化类型的判断以及有机结构的分析。


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 和
和
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:2011-2012学年宁夏银川一中高三(上)第四次月考化学试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com