
| A. | 葡萄糖、麦芽糖均能与银氨溶液反应 | |
| B. | 甘氨酸和丙氨酸缩合最多可以形成四种二肽 | |
| C. | 富含蛋白质的豆浆煮沸后即可得人体所需的氨基酸 | |
| D. | 油酯在氢氧化钾溶液中水解可制得汽车洗涤用的液体肥皂 |
分析 A.葡萄糖和麦芽糖均为还原性糖,均能与银氨溶液反应;
B.氨基酸形成肽键原理为羧基提供-OH,氨基提供-H,两个氨基酸分子脱去一个水分子脱水结合形成二肽,既要考虑不同氨基酸分子间生成二肽,又要考虑同种氨基酸分子间形成二肽;
C.蛋白质在加热条件下发生变性,而不是发生水解反应生成氨基酸;
D.油脂是高级脂肪酸甘油酯,油脂在碱性条件下发生皂化反应.
解答 解:A.葡萄糖和麦芽糖均为还原性糖,均能与银氨溶液反应,故A正确;
B.氨基酸生成二肽,就是两个氨基酸分子脱去一个水分子.当同种氨基酸脱水,生成2种二肽;当是异种氨基酸脱水:可以是甘氨酸脱去羟基,丙氨酸脱氢;也可以丙氨酸脱羟基,甘氨酸脱去氢,生成2种二肽,所以共有4种,故B正确;
C.蛋白质在加热条件下发生变性,需要在催化剂的作用下,蛋白质才会发生水解反应生成氨基酸,故C错误;
D.油脂是高级脂肪酸甘油酯,油脂在碱性条件下发生皂化反应,故D正确;
故选C.
点评 本题考查了糖类、油脂和蛋白质的结构、性质和用途,难度不大,B选项关键在于形成肽键既要考虑不同氨基酸分子间形成肽键,又要考虑同种氨基酸分子间形成肽键.


科目:高中化学 来源: 题型:解答题
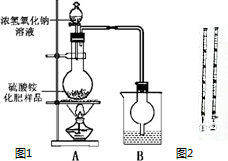 利用硫酸工业尾气中的二氧化硫可以制取氮肥硫酸铵.某探究小组设计实验对制得硫酸铵的品质进行鉴定.
利用硫酸工业尾气中的二氧化硫可以制取氮肥硫酸铵.某探究小组设计实验对制得硫酸铵的品质进行鉴定.| 指标 项目 | 优等品 | 一等品 | 合格品 |
| 外观 | 白色结晶,无可见机械杂质 | 无可见机械杂质 | |
| 氮(N)含量 | ≥21.0% | ≥21.0% | ≥20.5% |
| 滴定次数 | 滴定前读数/mL | 滴定后读数/mL |
| 1 | 1.20 | 18.91 |
| 2 | 0.00 | 18.60 |
| 3 | 1.10 | 18.79 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,1.12L1H2和0.2g 2H2均含有0.1NA个质子 | |
| B. | 在同压不同温的情况下,质量相同的氧气和臭氧所含氧原子数不相同 | |
| C. | 标准状况下,11.2L庚烷完全燃烧后生成的CO2分子数为3.5NA | |
| D. | 常温下,将5.6 g 铁投入足量的浓硫酸中转移电子数为0.3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2O3常用作红色油漆和涂料 | B. | 氟氯烃是安全、环保的制冷剂 | ||
| C. | 聚丙烯酸钠可做“尿不湿”原料 | D. | 硅胶可用作瓶装药品干燥剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12.4 g白磷中含有共价键数为0.4 NA | |
| B. | 3Fe+4H2O(g)=Fe3O4+4H2反应中,当5.6 g Fe全部转化为Fe3O4时,则有0.3 NA电子发生转移 | |
| C. | 在1 L 0.1 mol/L碳酸钠溶液中阴离子总数等于0.1 NA | |
| D. | 在标准状况下,22.4 L CH4与18 g H2O所含有的电子数均为10 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某密闭容器中的反应:3H2(g)+N2$?_{△}^{催化剂}$2NH3(g)△H<0,其正反应速率随时间变化的情况如图所示,判断下列有关t1时刻条件变化的说法可能正确的是( )
某密闭容器中的反应:3H2(g)+N2$?_{△}^{催化剂}$2NH3(g)△H<0,其正反应速率随时间变化的情况如图所示,判断下列有关t1时刻条件变化的说法可能正确的是( )| A. | 增大NH3浓度的同时减小N2浓度 | B. | 增大N2和H2的浓度 | ||
| C. | 扩大容器的体积 | D. | 降低反应温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 500 | 525 | 550 | 575 | 600 |
| 平衡转化率/% | 93.5 | 90.5 | 85.6 | 80.0 | 73.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲基的电子式是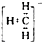 | B. | 硫的原子结构示意图是 | ||
| C. | ${\;}_{8}^{18}$O表示中子数是18的氧原子 | D. | 过氧化氢的结构式是H-O-O-H |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
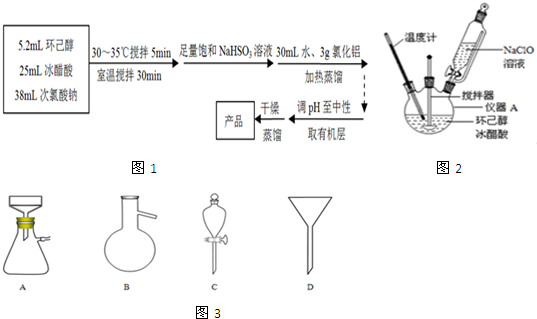

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com