
分析 溶液中离子的浓度=电解质的浓度×一个分子中含有的离子数目,据此计算出氯离子的物质的量浓度;根据稀释前后离子的浓度不变计算出稀释后Cl-的物质的量浓度.
解答 解:100ml0.25mol•L-1 AlCl3溶液中,Cl-的物质的量浓度为c(Cl-)=3c(AlCl3)=3×0.25mol/L=0.75mol/L;
设稀释后溶液中Cl-的物质的量浓度为c,则:0.75mol/L×0.1L=c×0.5L,解得c=0.15mol/L,
故答案为:0.75;0.15.
点评 本题考查物质的量浓度有关计算,题目难度不大,明确离子浓度与电解质的浓度、组成的关系为解答关键,注意溶液稀释前后溶质的物质的量不变.


科目:高中化学 来源: 题型:选择题
| A. | 1L0.1mol•L-1FeCl3溶液中含有的Fe3+离子数目为0.1NA | |
| B. | 常温常压下,4.6gNO2和N2O4混合物中含有的原子总数为0.3NA | |
| C. | 1mol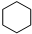 (环己烷)中含有6NA共价键 (环己烷)中含有6NA共价键 | |
| D. | 常温下,2.24LCl2完全与NaOH溶液反应,转移的电子数目一定为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
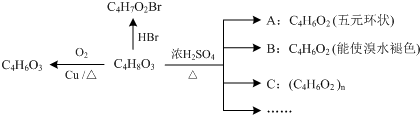
 .
. +H2O.
+H2O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “碳铵”的化学式:(NH4)2CO3 | |
| B. | 二氧化碳的结构式:O=C=O | |
| C. | 钾原子的结构示意图: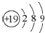 | |
| D. | 中子数为138、质子数为88的镭(Ra)原子:${\;}_{88}^{138}$Ra |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com