
在25°C、100 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,下列热化学方程式正确的是( )
A.CH3OH(l)+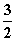 O2(g)===CO2(g)+2H2O(l) ΔH=725.8 kJ·mol-1
O2(g)===CO2(g)+2H2O(l) ΔH=725.8 kJ·mol-1
B.2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH=-1 452 kJ·mol-1
C.2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH=-725.8 kJ·mol-1
D.2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH=1 452 kJ·mol-1
科目:高中化学 来源: 题型:
海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
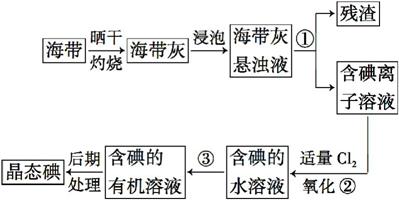
(1)步骤①的实验操作名称是 ;
(2)现有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品。完成该实验尚缺少的玻璃仪器是 ;
(3)步骤③中能选用CCl4从碘水中萃取碘的原因是 ;
A.CCl4与水不互溶
B.CCl4可与I2发生取代反应
C.CCl4的密度比水大
D.CCl4不易燃烧,可作灭火剂
E.碘在CCl4中的溶解度比在水中大很多
(4)步骤③中还可选择 作萃取剂;
(5)步骤②中反应的离子方程式是 ;
(6)请设计一种简单的实验方法,检验提取碘后的水溶液中是否还含有单质碘: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
新型材料纳米级铁粉与普通铁粉具有不同的性质。已知:在不同温度下,纳米级铁粉与水蒸气反应的固体产物不同,温度低于570℃时,生成FeO;高于570℃时,生成Fe3O4。
(1)写出温度低于570℃时反应的化学方程式 。
(2)中学教材中用右图所示实验装置,完成铁粉与水蒸气反应的演示实验。实验中使用肥皂液的作用是
。
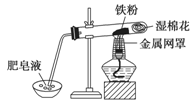
(3)如果提供给你3支试管、水槽、蒸发皿、胶塞、导管、酒精灯及其必要的仪器和物品,请在答题卷的方框中画出你设计的实验装置示意图发生该反应并有氢气的收集装置图(包括反应时容器中的物质)。

说明:①本题装置示意图中的仪器可以用下面的方式表示。
水槽:
 试管:
试管:
 蒸发皿:
蒸发皿:
 玻璃导管:
玻璃导管:
 或
或
 (但应标示出在液面上或液面下)
(但应标示出在液面上或液面下)
②铁架台、石棉网、酒精灯、玻璃导管之间的联接胶管等,在示意图中不必画出。如需加热,在需加热的仪器下方,标以“△”表示。
(4)乙同学为了探究实验后的固体产物是否存在Fe3O4(假定铁全部反应完全)设计下列实验方案:
①取固体样品m1 g,溶于足量的稀盐酸;
②向①反应后的溶液X中加入足量H2O2的和氨水,充分反应后,过滤、洗涤、干燥;
③将②中所得固体进行灼烧,得到红棕色固体m2 g。
溶液X中发生氧化还原反应的离子方程式为 ;m1与m2符合 关系时,才能确定固体样品中一定只存在Fe3O4。
查看答案和解析>>
科目:高中化学 来源: 题型:
在100 g碳不完全燃烧所得气体中,CO和CO2的体积比为1∶2,已知:
C(s)+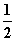 O2(g)===CO(g) ΔH1=-110.35 kJ·mol-1①
O2(g)===CO(g) ΔH1=-110.35 kJ·mol-1①
CO(g)+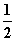 O2(g)===CO2(g) ΔH2=-282.57 kJ·mol-1②
O2(g)===CO2(g) ΔH2=-282.57 kJ·mol-1②
则与100 g碳完全燃烧相比,损失的热量是( )
A.392.92 kJ B.2 489.42 kJ C.784.92 kJ D.3 274.3 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对化学反应热问题的说法正确的是( )
A.放热反应发生时不必加热
B.化学反应一定有能量变化
C.一般地说,吸热反应加热后才能发生
D.化学反应的热效应数值与参加反应的物质的多少无关
查看答案和解析>>
科目:高中化学 来源: 题型:
利用如图装置测定中和热的实验步骤如下:
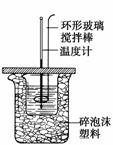
①用量筒量取50 mL 0.25 mol·L-1硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50 mL 0.55 mol·L-1 NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度。
回答下列问题:
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3 kJ·mol-1):________________________________________________________________________
________________________________________________________________________。
(2)倒入NaOH溶液的正确操作是______(从下列选出)。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)使硫酸与NaOH溶液混合均匀的正确操作是______(从下列选出)。
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(4)实验数据如下表:
①请填写下表中的空白:
| 温度 实验次数 | 起始温度t1℃ | 终止温 度t2/℃ | 温度差平均值(t2-t1) /℃ | |
| H2SO4 | NaOH | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 |
②近似认为0.55 mol·L-1 NaOH溶液和0.25 mol·L-1硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18 J·g-1·℃-1。则中和热ΔH=
________________________________________________________________________
( 取小数点后一位)。
③上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是(填字母)
____________。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
已知电极材料:铁、铜、银、石墨、锌、铝;电解质溶液:CuCl2溶液、Fe2(SO4)3溶液、硫酸。按要求回答下列问题:
(1)电工操作上规定:不能把铜导线和铝导线连接在一起使用。请说明原因________________________________________________________________________。
(2)若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线,能否构成原电池?________。若能,请写出电极反应式,负极:____________________,正极:________________________。(若不能,后两空不填)
(3)设计一种以铁和稀硫酸反应为原理的原电池,要求画出装置图(需标明电极材料及电池的正、负极)。
查看答案和解析>>
科目:高中化学 来源: 题型:
在加入铝粉能产生H2的溶液中,下列各组离子可能大量共存的是( )
A.NH4+ NO3- CO32- Na+
B.Na+ Ba2+ Mg2+ HCO3-
C.NO3- Mg2+ K+ Cl-
D.NO3- K+ [Al(OH)4]- OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com