
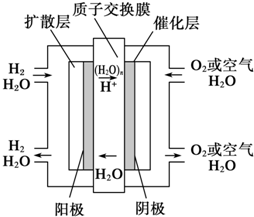
 Ϊ���֡���������������á������⣬�Ϻ���������ŵ�������ڽ�ͨ�����ŷš������ܱ߽�ͨ�����ŷš���2010��4��15������Դ��������ʽ���������У��ó�װ�š���ɫ���ࡱ--���ӽ���Ĥȼ�ϵ�أ��乤��ԭ����ͼ��ʾ������������ȷ���ǣ�������
Ϊ���֡���������������á������⣬�Ϻ���������ŵ�������ڽ�ͨ�����ŷš������ܱ߽�ͨ�����ŷš���2010��4��15������Դ��������ʽ���������У��ó�װ�š���ɫ���ࡱ--���ӽ���Ĥȼ�ϵ�أ��乤��ԭ����ͼ��ʾ������������ȷ���ǣ�������| A��ͨ�������ĵ缫����������Ӧ | ||||
| B��ͨ�������ĵ缫Ϊ���� | ||||
C���ܷ�ӦʽΪO2+2H2
| ||||
| D�������ĵ缫��ӦʽΪO2+4H++4e-�T2H2O |


 ֥�鿪���γ�������ϵ�д�
֥�鿪���γ�������ϵ�д� ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����NH4��2Cr2O7=N2��+Cr2O3+4H2O |
| B��2Cu+O2+CO2+H2O=Cu��OH��2CO3 |
| C��NH4NO3=N2O��+2H2O |
| D��Cu2��OH��2CO3=2CuO+H2O+CO2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
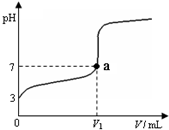 �����£���20mL x mol?L-1 CH3COOH��Һ����μ�������ʵ���Ũ�ȵ�NaOH��Һ�����Һ��pH��NaOH��Һ�������V���仯��ϵ��ͼ��ʾ�������¶ȱ仯��������˵���в���ȷ���ǣ�������
�����£���20mL x mol?L-1 CH3COOH��Һ����μ�������ʵ���Ũ�ȵ�NaOH��Һ�����Һ��pH��NaOH��Һ�������V���仯��ϵ��ͼ��ʾ�������¶ȱ仯��������˵���в���ȷ���ǣ�������| A������ CH3COOH��Һ�У�c��H+��=1��10-3mol?L-1 |
| B��ͼ��V1��20 mL |
| C��a���Ӧ����Һ�У�c��CH3COO-��=c��Na+�� |
| D��������NaOH��Һ�����Ϊ20 mLʱ����Һ�У�c��CH3COOH��+c��H+��=c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1��6 | B��6��1 |
| C��2��3 | D��1��5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ˮ�к�����Ԫ�أ�ֻ�辭�������仯�Ϳ��Եõ������� |
| B����ˮ�����Ƶô��Σ����ᴿ���ٵ������Һ���Եõ������� |
| C���Ӻ�ˮ���ᴿ����ʳ�Σ���ⱥ��ʳ��ˮ�����IJ�������Ƶ�84����Һ��NaClO�� |
| D������ͨ����������ֱ�ӴӺ�ˮ����ȡ�嵥�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��250mL 0.4mol/L��ϡ������Һ |
| B��25mL 0.8mol/L��ϡ������Һ |
| C��100mL 1mol/L��ϡ������Һ |
| D��100mL 2mol/L��������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
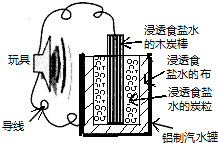 ��ͼ��һ���÷Ͼɲ��������Ŀ�����������ߵĵ��ʾ��ͼ���õ�ع���ʱ���й�˵����ȷ���ǣ�������
��ͼ��һ���÷Ͼɲ��������Ŀ�����������ߵĵ��ʾ��ͼ���õ�ع���ʱ���й�˵����ȷ���ǣ�������| A��ľ̿��Ӧ����ߵ���ĸ������� |
| B��̿����̿���Ϸ����ĵ缫��Ӧ�ǣ�O2+4e-=2O2- |
| C����������ʴ |
| D����Ϊһ��ʼ��Ӧ�ͻ����ɴ����������õ����һ����Σ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��H2O��Al3+ |
| B��Cl-��Na+ |
| C��O2��CO2 |
| D��NH3��CO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ����ʽ | N2+3H2?2NH3 | ||
| ��ʼŨ��/mol?L-1 | 1.0 | 3.0 | 0 |
| 3��ĩŨ��/mol?L-1 | 0.6 | 1.8 | 0.8 |
| A��0.2 mol?L-1?s-1 |
| B��0.3 mol?L-1?s-1 |
| C��0.4 mol?L-1?s-1 |
| D��0.6mol?L-1?s-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com