
有0.1 mol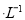 的三种溶液:①CH3COOH、②NaOH、③CH3COONa,下列说法正确的是
的三种溶液:①CH3COOH、②NaOH、③CH3COONa,下列说法正确的是
A.溶液①中,C(CH3COO-)=C(H+)
B.溶液①、②等体积混合,混合液中c(CH3COO-)等于溶液③中的C(CH3COO-)
C.溶液①、②等体积混合,混合液中c(CH3COO-)+ c(CH3COOH)= C(Na+)
D.溶液①、③等体积混合,混合液中C(Na+)>C(CH3COO-)> C(H+)>C(OH-)
C
【解析】
试题分析:A、溶液①中,醋酸电离产生的C(CH3COO-)=C(H+),但溶液中的C(CH3COO-)<C(H+),错误;B、溶液①、②等体积混合,混合液的CH3COONa的浓度为0.05 mol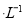 ,所以混合液中c(CH3COO-)小于溶液③中的C(CH3COO-),错误;C、溶液①、②等体积混合,混合液的CH3COONa的浓度为0.05 mol
,所以混合液中c(CH3COO-)小于溶液③中的C(CH3COO-),错误;C、溶液①、②等体积混合,混合液的CH3COONa的浓度为0.05 mol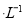 ,根据物料守恒规律,有c(CH3COO-)+ c(CH3COOH)= C(Na+)=0.05 mol
,根据物料守恒规律,有c(CH3COO-)+ c(CH3COOH)= C(Na+)=0.05 mol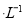 ,正确;D、溶液①、③等体积混合,溶液为酸性,所以C(CH3COO-)> C(Na+),错误,答案选C。
,正确;D、溶液①、③等体积混合,溶液为酸性,所以C(CH3COO-)> C(Na+),错误,答案选C。
考点:考查混合液中的离子浓度的大小比较,守恒规律的应用


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2013-2014天津市高一下学期期中考试化学试卷(解析版) 题型:选择题
运用元素周期律分析下列推断,其中错误的是
A.铍是一种轻金属,它的氧化物的水化物可能具有两性
B.砹单质是一种有色固体,砹化氢很不稳定
C.硒化氢(H2Se)是无色、有毒、比H2S稳定的气体
D.硫酸锶难溶于水
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市河北区高三总复习质量检测一理综化学试卷(解析版) 题型:选择题
下列选项中所涉及的两个量一定相等的是
A.电解精炼铜时阳极溶解与阴极析出的铜的质量
B.6.2gNa2O 和7.8gNa2O2 中所含的离子数
C.11.2 LN2与14gCO气体所含有的原子数
D.20g重水(D2O)与34gNH3 所含有的电子数
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市河东区高三二模考试理综化学试卷(解析版) 题型:填空题
(14分)X、Y、Z、W、P为短周期的主族元素,其原子序数依次增大。Y、Z、W、P位于同一周期。X 元素形成的单质是自然界中含量最多的气体,1mol Y的单质分别与足量盐酸和氢氧化钠溶液反应生成的气体在标况下均为33.6L。W的原子最外层电子数与核外电子总数之比为3:8,X的原子序数是Z的原子序数的一半。
(1)Y在周期表中的位置是________;X的氢化物与P的氢化物接近时的现象是_________。
(2)W与P可形成原子个数比为1:2的化合物,其电子式为__________。
(3)Y与P形成的化合物溶液显____性;用离子反应方程式表示显这种性质的原因________________。
(4)Z、W、P三种元素的气态氢化物稳定性由高到低的顺序是______________________(填化学式)。
(5)X的三氟化物是微电子工业中优良的等离子刻蚀气体,但在潮湿的环境中能与水发生反应生成无色气体,遇空气变为红棕色。写出此三氟化物与水反应的化学反应方程式_____,若0.6mol X的三氟化物完全与水反应,则转移的电子总数约为_________个。
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市河东区高三一模理综化学试卷(解析版) 题型:填空题
(14分)氮的化合物是中学化学的重要物质,与人类生活密切相关。
(1)金属与不同密度的硝酸溶液反应所得的还原产物比较复杂,如图所示:
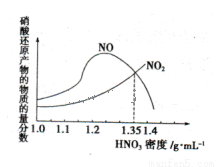
请写出铁与密度为1.35 g.m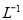 的硝酸反应的化学方程式:______________________.
的硝酸反应的化学方程式:______________________.
(2)亚硝酸钠是一种致癌物质,它在中性或碱性条件下是稳定的,酸化后能氧化碘化钾生成棕色溶液和NO,则该反应中氧化剂与还原剂的物质的量之比为____。
(3)如图甲为NO2和C0反应生成CO2和NO过程的能量变化示意图,请写出该反应的热化学方程式:__________________________________________________________.
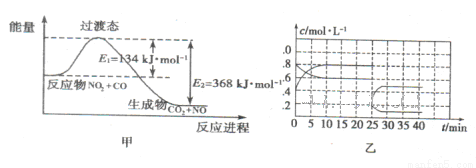
(4)已知NO2和N2O4可以相互转化:2NO2(g)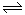 N2O4(g) △H<0。现将一定量的NO2和N2O4混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物的浓度随时问变化关系如图乙所示。
N2O4(g) △H<0。现将一定量的NO2和N2O4混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物的浓度随时问变化关系如图乙所示。
①前10 min内用NO2表示的平均反应速率v(NO2)= ;上述反应的平衡常数K=__________。
②反应进行至25 min时,曲线发生变化的原因是________________________.
③若要使上述反应的平衡常数K增大,采取的措施是_________________。
A.加入催化剂B.缩小容器体积C.降低温度 D.再加入一定量的NO2
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市高三第五次月考理综化学试卷(解析版) 题型:填空题
(14分)甲醇、二甲醚等被称为绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚(CH3OCH3)。
(1)已知1g二甲醚气体完全燃烧生成稳定的氧化物放出的热量为32kJ,请写出二甲醚燃烧热的热化学方程式____________________________________________________________________。
(2)写出二甲醚碱性燃料电池的负极电极反应式 __________________________________。
(3)用合成气制备二甲醚的反应原理为:2CO(g) + 4H2(g) CH3OCH3(g) + H2O(g)。已知一定条件下,该反应中CO的平衡转化率随温度、投料比[n(H2) / n(CO)]的变化曲线如下左图:
CH3OCH3(g) + H2O(g)。已知一定条件下,该反应中CO的平衡转化率随温度、投料比[n(H2) / n(CO)]的变化曲线如下左图:
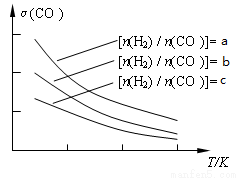
①a、b、c按从大到小的顺序排序为_________________,该反应的△H_______0(填“>”、“<”)。
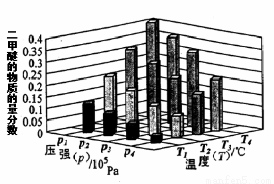
②某温度下,将2.0molCO(g)和4.0molH2(g)充入容积为2L的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中CH3OCH3(g)的物质的量分数变化情况如上图所示,关于温度和压强的关系判断正确的是 ;
A. P3>P2,T3>T2 B. P1>P3,T1>T3 C. P2>P4,T4>T2 D. P1>P4,T2>T3
③在恒容密闭容器里按体积比为1:2充入一氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是 ;
A. 正反应速率先增大后减小 B. 逆反应速率先增大后减小
C. 化学平衡常数K值减小 D. 氢气的转化率减小
④ 某温度下,将4.0molCO和8.0molH2充入容积为2L的密闭容器中,反应达到平衡时,测得二甲醚的体积分数为25%,则该温度下反应的平衡常数K=__________。
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市高三第五次月考理综化学试卷(解析版) 题型:选择题
下列物质的转化在给定条件下能实现的是
①SiO2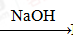 Na2SiO3
Na2SiO3 H2SiO3 ②Fe
H2SiO3 ②Fe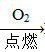 Fe2O3
Fe2O3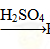 Fe2(SO4)3
Fe2(SO4)3
③BaSO4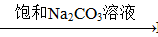 BaCO3
BaCO3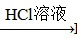 BaCl2 (Ksp(BaSO4)=1.1×10-10 Ksp(BaCO3)=2.6×10-9)
BaCl2 (Ksp(BaSO4)=1.1×10-10 Ksp(BaCO3)=2.6×10-9)
④AlCl3溶液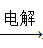 Al
Al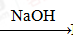 NaAlO2
NaAlO2
⑤HCHO HCOOH
HCOOH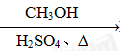 HCOOCH3
HCOOCH3
A.①②⑤ B.②③④ C.②④⑤ D.①③⑤
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市第二学期期中检测高一化学试卷(解析版) 题型:选择题
可用于电动汽车的铝—空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极。下列说法正确的是
A.以NaCl溶液或NaOH溶液为电解液时,正极反应式都为:O2+2H2O+4e-===4OH-
B.以NaOH溶液为电解液时,负极反应式为Al+3OH--3e-===Al(OH)3
C.以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变
D.电池工作时,电子通过外电路从正极流向负极
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市下学期期中考试高二化学试卷(解析版) 题型:选择题
下列实验中,不能达到预期目的是
①苯、浓溴水、溴化铁混合制溴苯
②乙醇和30%的硫酸共热到170℃制乙烯
③用溴水除去混在苯中的己烯,分液得到纯净的苯
④敞口久置的电石与饱和食盐水混合制乙炔
⑤将电石与水反应产生的乙炔通入溴水中,溴水褪色,证明乙炔和溴水发生了加成反应
⑥将溴乙烷和NaOH乙醇溶液混合共热,生成的气体直接通入酸性高锰酸钾溶液,酸性高锰酸钾溶液褪色,说明有乙烯生成
A. ②④⑥ B.①③⑤ C.①②④⑥ D.①②③④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com