

分析 以菱镁矿(主要成分为MgCO3,SiO2和FeCO3)为原料,加入稀硫酸酸溶过滤得到滤液为硫酸镁,硫酸亚铁溶液,滤渣1为SiO2,滤液中加入过氧化氢氧化亚铁离子为铁离子,加入一水合氨调节溶液pH沉淀铁离子,过滤得到滤渣2为Fe(OH)3沉淀,滤液为硫酸镁溶液,蒸发浓缩,冷却结晶,过滤洗涤制备硫酸镁,和木炭高温煅烧制备高纯氧化镁,以此来解答.
解答 解:(1)MgCO3与稀硫酸反应生成硫酸镁、二氧化碳和水,化学方程式为:MgCO3+H2SO4═MgSO4+CO2↑+H2O,反应的离子方程式为MgCO3+2H+═Mg2++CO2↑+H2O,
故答案为:MgCO3+2H+═Mg2++CO2↑+H2O;
(2)加入H2O2 氧化时,在酸性溶液中氧化硫酸亚铁为硫酸铁,反应的化学方程式为2FeSO4+H2O2+H2SO4═Fe2(SO4)3+2H2O,离子反应为2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(3)由上述分析可知,滤渣1和滤渣2的成分别是SiO2、Fe(OH)3,
故答案为:SiO2、Fe(OH)3;
(4)①上述煅烧过程中产生的SO2用溴水吸收,离子方程式为SO2+Br2+2H2O═4H++2Br-+SO42-,
故答案为:SO2+Br2+2H2O═4H++2Br-+SO42-;
②淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,由氧化还原反应原理,可知最低价为-2价,反应的离子方程式为3S+6OH-$\frac{\underline{\;\;△\;\;}}{\;}$2S2-+SO32-+3H2O,
故答案为:3S+6OH-$\frac{\underline{\;\;△\;\;}}{\;}$2S2-+SO32-+3H2O.
点评 本题考查物质的制备实验,为高频考点,把握制备实验流程、物质的性质及发生的反应为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合,该实验题对氧化还原反应、离子方程式书写的要求较高,题目难度不大.


科目:高中化学 来源: 题型:多选题
| A. | 反应前盐酸的温度 | B. | 反应前盐酸的质量 | ||
| C. | 反应前氢氧化钠溶液的温度 | D. | 反应前氢氧化钠溶液的质量 | ||
| E. | 反应后混合溶液的最高温度 | F. | 反应后混合溶液的质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 科学家正在研究温室气体CH4和CO2的转化和利用.
科学家正在研究温室气体CH4和CO2的转化和利用.| 参数 分子 | 分子直径/nm | 分子与H2O的 结合能E/kJ•mol-1 |
| CH4 | 0.436 | 16.40 |
| CO2 | 0.512 | 29.91 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 原子序数依次增大的A、B、C、D、E、F六种元素.其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A 原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的 原子序数为29.
原子序数依次增大的A、B、C、D、E、F六种元素.其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A 原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的 原子序数为29.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处.在一定条件下发生可逆反应:2A(g)+B(g)?2C(g); 反应达到平衡后,再恢复至原温度.回答下列问题:
如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处.在一定条件下发生可逆反应:2A(g)+B(g)?2C(g); 反应达到平衡后,再恢复至原温度.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
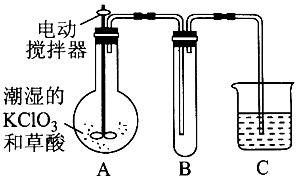
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Mg2+ | 8.1 | 9.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com