
(14分,每空2分))镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2碳粉氧化铁等涂覆在铝箔上制成。由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行资源回收研究,设计实验流程如下:
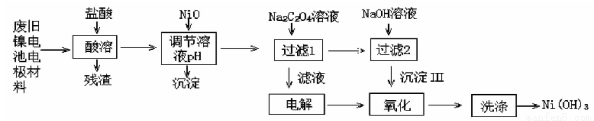
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+。
②已知实验温度时的溶解度:NiC2O4> NiC2O4·H2O > NiC2O4·2H2O
③Ksp[Ni(OH)2]=5.0×10-16, Ksp(NiC2O4)=5.0×10-10;
回答下列问题:
(1)酸溶后所留残渣的主要成分为 (填物质名称)。
(2)用NiO调节溶液的pH,析出沉淀的成分为 (填化学式)。
(3)写出加入Na2C2O4溶液后反应的化学方程式: 。
(4)写出加入NaOH溶液所发生反应的离子方程式: 。
(5)电解过程中阴极反应式 ,沉淀Ⅲ可被电解所得产物之一氧化,写出氧化反应的离子方程式 。
(6)铁镍蓄电池,放电时总反应为:
Fe+Ni2O3+3H2O=Fe(OH)2+2Ni(OH)2,下列有关该电池的说法不正确的是
A.电池的电解液为碱性溶液,正极为Ni2O3负极为Fe
B.电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2
C.电池充电过程中,阴极附近溶液的pH降低
D.电池充电时,阳极反应为2Ni(OH)2+2OH--2e-=Ni2O3+3H2O
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014-2015学年甘肃省天水市秦安县高三第一次模拟考试化学试卷(解析版) 题型:选择题
下列反应的离子方程式书写正确的是
A.含等物质的量的MgCl2、Ba(OH)2、HNO3三种溶液混合:Mg2+ + 2OH- = Mg(OH)2↓
B.CaCO3溶于CH3COOH:CaCO3 + 2CH3COOH = Ca2+ + 2CH3COO- + CO2↑ + H2O
C.过量HI溶液加入到Fe(NO3)3溶液中:2Fe3+ + 2I- = 2Fe2+ + I2
D.SO2通入到溴水中:SO2 + H2O + Br2 = 2H+ + SO42- + 2Br-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省合肥市高三第二次教学质量检测理综化学试卷(解析版) 题型:填空题
(14分)硫代硫酸钠是一种常见的化工原料,将SO2通入按一定比例配成的Na2S和Na2CO3的混合溶液中,便可得到Na2S2O3,其制备反应方程式为:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2
(1)在配制混合溶液前先将蒸馏水加热煮沸一段时间后待用,其目的是 。
(2)用该方法获得的Na2S2O35H2O晶体中常混有一定量的杂质,某兴趣小组欲对其中所含杂质成分进行探究。
【提出假设】该晶体中含有的杂质可能是:Na2CO3、Na2SO3、_____、_____等中的一种或几种,若晶体中混有Na2SO3,则生成Na2SO3的化学方程式为 。
【判断与思考】
某同学取少量制得的晶体溶于足量稀硫酸,并将产生的气体通入CuSO4溶液中,未见黑色沉淀,据此认为晶体中一定不含Na2S,你认为其结论是否合理?_______ (填“合理”、“不合理”)并说明理由:______________
【设计方案进行实验】
若检验晶体中含Na2CO3,完成下表实验方案、现象及结论(仪器自选)。
限选实验试剂:3mol/LH2SO4、1mol/LNaOH酸性KMnO4溶液、饱和NaHCO3溶液、品红溶液、澄清石灰水

(3)已知:2 Na2S2O3+I2=2NaI+Na2S4O6。为测定所制得晶体的纯度,该小组以淀粉作指示剂,用0.010mol/L 的碘水进行多次取样滴定,测得Na2S2O35H2O的含量约为102%。若所用试剂及操作均无不当,产生该结果最可能的原因是______________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省上饶市高三上学期第一次联考化学试卷(解析版) 题型:选择题
有一种铁的“氧化物”样品,用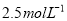 盐酸
盐酸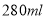 恰好完全溶解,所有溶液还能吸收标况下的0.56L氯气,如使其中的
恰好完全溶解,所有溶液还能吸收标况下的0.56L氯气,如使其中的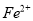 全部转化为
全部转化为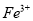 ,该样品可能的化学式是
,该样品可能的化学式是
A.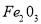 B.
B.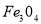 C.
C.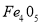 D.
D.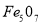
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省上饶市高三第二次高考模拟化学试卷(解析版) 题型:推断题
(15分,除标明外,其余每空2分)吡洛芬是一种用于治疗风湿病的药物。它的合成路线如下:

回答下列问题:
(1)B→C的反应类型为 。
(2)A→B的化学方程式为 。从整个合成路线看,步骤A→B的目的是 。
(3)E的结构简式为 。
(4)A在一定条件下可生成F( )。写出同时满足下列条件的F的两种同分异构体的结构简式: 。
)。写出同时满足下列条件的F的两种同分异构体的结构简式: 。
①属于芳香族化合物
②是一种α-氨基酸
③分子中有6种不同化学环境的氢原子
(5)非那西汀是一种解热药,其结构简式为 。写出以苯酚钠CH3CH2OH和(CH3CO)2O为原料制备非那西汀的合成路线流程图(无机试剂任用)。
。写出以苯酚钠CH3CH2OH和(CH3CO)2O为原料制备非那西汀的合成路线流程图(无机试剂任用)。
合成路线流程图示例如下:
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省上饶市高三第二次高考模拟化学试卷(解析版) 题型:选择题
X.YZW是原子序数依次增大的四种短周期元素,甲乙丙丁戊是由其中的两种或三种元素组成的化合物,己是由Z元素形成的单质。已知:甲+乙→丁+己,甲+丙→戊+己;0.1mol·L-1丁溶液的pH为13(25℃)。下列说法正确的是
A.1mol甲与足量的乙完全反应共转移2mol电子
B.Y元素在周期表中的位置为第3周期ⅣA族
C.原子半径:W>Y>Z>X
D.1.0L0.1mol·L-1戊溶液中阴离子总的物质的量小于0.1mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省无锡市高三期末考试化学试卷(解析版) 题型:填空题
(12分)锂/磷酸氧铜电池是一种以磷酸氧铜作为正极材料的锂离子电池,其正极的活性物质是Cu4O(PO4)2,制备流程如下:
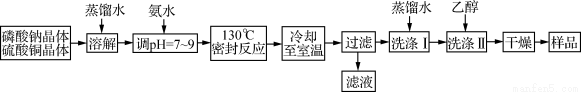
主要反应原理:2Na3PO4+4CuSO4+2NH3·H2O===Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)实验室进行“过滤”操作使用的玻璃仪器主要有________。
(2)流程中“洗涤Ⅰ”后,检验沉淀已洗涤干净的方法是____________________。
(3)该电池放电时,负极锂转化为Li2O,正极磷酸氧铜转变为Cu和Li3PO4,写出该电池放电时的化学方程式____________________。
(4)准确称取上述流程所得的样品38.56 g[假定样品中只含Cu4O(PO4)2和CuO两种物质],使其完全溶于一定量的硝酸中,再加入氢氧化钠溶液,使铜完全沉淀,将沉淀灼烧使其转变为黑色氧化铜,最终称得残留固体质量为27.20 g。计算所得样品中磷酸氧铜的质量分数。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省无锡市高三期末考试化学试卷(解析版) 题型:选择题
2014年11月APEC会议期间,北京市区天空湛蓝,PM2.5浓度为每立方米37微克,接近一级优水平。网友形容此时天空的蓝色为“APEC蓝”。下列有关说法不正确的是
A.开发新能源,如太阳能、风能等,减少对化石能源的依赖
B.直径接近于2.5×10-6m的颗粒物(PM2.5)分散在空气中形成的混合物具有丁达尔效应
C.燃煤进行脱硫脱硝处理,减少硫的氧化物和氮的氧化物的排放
D.通过吸收空气中CO2并利用廉价能源合成汽油可推广“绿色自由”计划
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省哈尔滨市高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列化合物分子中,在核磁共振氢谱图中能给出三种信号的是
A.CH3CH2CH3 B.CH3CH2COCH2CH3
C.CH3CH2OH D.CH3OCH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com