
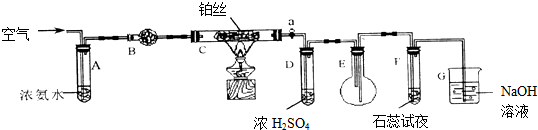
���� Ũ��ˮ�ӷ�������������ӷ���Ũ��ˮ����Bװ�ã�B�еļ�ʯ���������ﰱ��������İ�����C�з�������������һ��������ˮ����Ũ�����������ɵ�ˮ��ʣ������һ��������E��������������������Ӧ���ɺ���ɫ�Ķ�������������������F�е�ˮ�������ᣬ��Һ�����ԣ��ܹ�ʹʯ����ɫ�����������������Һ���չ����Ķ���������
��1��������֪װ��B���Ǽ�ʯ�ң�
��2�������Ĵ�������Ӧ�Ƿ��ȷ�Ӧ��
��3�������Ĵ���������һ��������ˮ������װ��C���������廹�а���������Ũ���ᷴӦ���ɹ�������臨��������ܣ���Ҫͨ��ˮ���գ�
��4��һ����������װ��E�кͿ����е�������Ӧ���ɺ���ɫ�������������Gװ������������Һ������ʣ�൪�����
��5��װ��E�����ɵĶ�����������װ��F��ˮ��Ӧ���������һ��������ʹʯ����Һ���ɫ��
��6������߹�ҵ�ϳɰ�ת���ʣ�Ӧʹ��ѧƽ��������У�
��N2+3H2$\frac{\underline{\;\;����\;\;}}{���¸�ѹ}$2NH3 ��H��0���÷�Ӧ�����������С�����ȵĿ��淴Ӧ��Ҫʹƽ��������Ӧ�����ƶ���Ӧ�����¶ȡ�����ѹǿ���¶ȹ��ͷ�Ӧ���ʹ�С���¶�Խ�ߣ���Ӧ����Խ��ʹ�ô���Ҳ������Ӧ���ʣ����ݴ����Ļ������¶�Ӱ�����������������
��� �⣺��1������������֪װ��B���Ǽ�ʯ�ң��������ջ�������е�ˮ�����ʴ�Ϊ����ʯ�ң�
��2����ʱ�����������˿�ֱ���ȣ�˵�������Ĵ������Ƿ��ȷ�Ӧ���ʴ�Ϊ�����ȣ�
��3�������Ĵ���������һ��������ˮ������װ��C���������廹�а���������Ũ���ᷴӦ���ɹ�������臨��������ܣ������Ǽ������壬Ũ�����ӷ����Ȼ������壬����װ��F�е�ʵ������ʯ�Ҳ������հ�����������������ˮ��������Ҫͨ��ˮ���գ���ѡ�٣�
�ʴ�Ϊ���٣�
��4��һ����������װ��E�кͿ����е�������Ӧ���ɺ���ɫ�������������Gװ������������Һ������ʣ�൪�������ֹ��Ⱦ������
�ʴ�Ϊ������ɫ������β����ֹ��Ⱦ������
��5��װ��E�����ɵĶ�����������װ��F��ˮ��Ӧ���������һ��������3NO2+H2O=2HNO3+NO������ʹʯ����Һ���ɫ���ʴ�Ϊ��3NO2+H2O=2HNO3+NO��
��6������߹�ҵ�ϳɰ�ת���ʣ�Ӧʹ��ѧƽ��������У�N2+3H2$\frac{\underline{\;\;����\;\;}}{���¸�ѹ}$2NH3 ��H��0���÷�Ӧ�����������С�����ȵĿ��淴Ӧ��Ҫʹƽ��������Ӧ�����ƶ���Ӧ�����¶ȡ�����ѹǿ��
a������ѹǿ��ƽ��������У���Ӧ��ת��������a��ȷ��
b�������¶�ƽ��������У���Ӧ��ת���ʼ�С����b����
c��ʹ������ý�ı䷴Ӧ���ʣ����ı仯ѧƽ�⣬ת���ʲ��䣬��c����
d�������ɵ�NH3��ʱ�ӻ�������з����ȥ��ƽ��������У���Ӧ��ת��������d���ϣ�
�ʴ�Ϊ��ad��
��N2+3H2$\frac{\underline{\;\;����\;\;}}{���¸�ѹ}$2NH3 ��H��0���÷�Ӧ�����������С�����ȵĿ��淴Ӧ��Ҫʹƽ��������Ӧ�����ƶ���Ӧ�����¶ȡ�����ѹǿ�����¶ȹ��ͷ�Ӧ���ʹ�С�������ڹ�ҵ����Ч�棻�¶�Խ�ߣ���Ӧ����Խ������Ӧ�ʵ������¶ȣ�ʹ��Ӧ��������ʹ�ô���Ҳ������Ӧ���ʣ�����500������ʱ�����Ļ����������ѡ�����500�����ҵ��¶Ƚ��У�
�ʴ�Ϊ���ʵ������¶ȣ�ʹ��Ӧ����������500������ʱ�����Ļ������
���� ����Ϊʵ���⣬������ʵ����Ʒ��������ۣ��������ʵ�����Ӧ�ã���ȷʵ��ԭ������װ�õ������ǽ���ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | Cu��OH��2 | Fe��OH��3 | CuCl | CuI |
| Ksp | 2.2��10-20 | 2.6��10-39 | 1.7��10-7 | 1.3��10-12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����粒�����n��NH4+����n��SO42-�� | |
| B�� | ��ͬ�¶��£�0.01mol/L�Ĵ�����Һ��0.02mol/L ������Һ�е�c��H+�� | |
| C�� | Һ����ڡ�0���̶�ʱ��50mL��ʽ�ζ��ܺ�25mL��ʽ�ζ�������ʢ��Һ����� | |
| D�� | �������Һ�У�c��NH4+����c��SO42-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ijУ��ѧ�о���ѧϰС����Ũ������������̼��ȷ�Ӧ����ȡ���ռ�������װ����ͼ��
ijУ��ѧ�о���ѧϰС����Ũ������������̼��ȷ�Ӧ����ȡ���ռ�������װ����ͼ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com