

|
 CuSO4+SO2↑+2H2O ( 2分) 长导管(1分)
CuSO4+SO2↑+2H2O ( 2分) 长导管(1分) CuSO4+SO2↑+2H2O。再加热的条件下,水蒸气易挥发,所以利用长导管,起冷凝回流作用。
CuSO4+SO2↑+2H2O。再加热的条件下,水蒸气易挥发,所以利用长导管,起冷凝回流作用。

科目:高中化学 来源:不详 题型:单选题
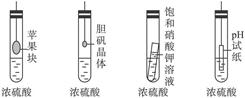
| A.苹果块会干瘪 | B.胆矾晶体表面有“白斑” |
| C.小试管内有晶体析出 | D.pH试纸变红 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 物质 | 溶解度(g/100水) | 物质 | 溶解度(g/100水) |
| Ca(OH)2 | 0.173 | Ba(OH)2 | 3.89 |
| CaCO3 | 0.0013 | BaSO3 | 0.016 |
| Ca(HCO3)2 | 16.60 | | |
| 实验方案 | 现象 |
| 方案1:取少量溶液于试管中,加入稀盐酸,加热,用①检验产生的气体。 | ② |
| 方案2:取少量溶液于试管中,加入③ 溶液并观察现象。 | ④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
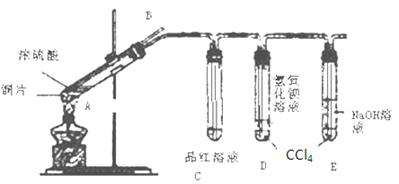
| A.通过品红溶液,若品红溶液褪色,则说明混有CO2气体 |
| B.通过澄清石灰水,若变混浊,则说明混有CO2气体 |
| C.先通过足量NaOH溶液,再通过澄清石灰水,若变混浊,则说明混有CO2气体 |
| D.先通过足量KMnO4溶液(具有强氧化性),再通过澄清石灰水,若变混浊,则说明混有CO2气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
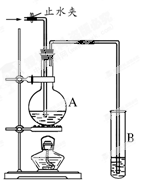
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.两种气体都生成BaSO4沉淀 |
| B.只有SO3会生成BaSO4沉淀,SO2通入溶液中无沉淀生成 |
| C.分别生成BaSO3和BaSO4两种沉淀 |
| D.都不生成沉淀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.浓H2SO4有氧化性,稀H2SO4无氧化性 |
| B.由于浓H2SO4具有脱水性,所以可用做干燥剂 |
| C.稀H2SO4与铜不反应,浓H2SO4在加热条件下可与铜反应 |
| D.在受热的情况下浓硫酸也不与铁、铝发生反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SO2使品红溶液和溴水褪色,说明SO2具有漂白性 |
| B.BaSO4不溶于水和酸,在医学上可用作钡餐 |
| C.洒落在地上的汞可在其表面撒硫磺除去 |
| D.蔗糖加入浓硫酸后变黑,说明浓硫酸具有脱水性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com