
【题目】废弃物的综合利用既有利于节约资源,又有利于保护环境。实验室利用废弃旧电池的铜帽(Zn、Cu总含量约为99%)回收铜并制备ZnO的部分实验过程如下:
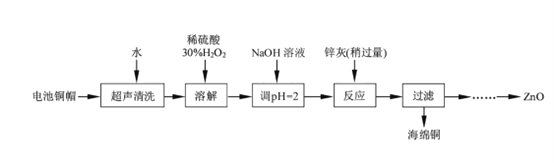
(1)①铜帽溶解时加入H2O2的目的是_______________(用化学方程式表示)。
②铜帽溶解后需将溶液中过量H2O2除去。除去H2O2的简便方法是_________________。
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)含量,实验中需测定除去H2O2后溶液中Cu2+的含量。实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节pH=3~4,加入过量KI,用Na2S2O3标准溶液滴定至终点。上述过程中的离子方程式如下:2Cu2++4I-=2CuI(白色)↓+I2、I2+2S2O32-=2I-+S4O62-
①滴定选用的指示剂为________________,滴定终点观察到的现象为________________。
②若滴定前溶液中H2O2没有除尽,所测定的Cu2+的含量将会______________(填“偏高”“偏低”“不变”)。
(3)已知pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了几种离子生成氢氧化物沉淀pH(开始沉淀的pH按金属离子浓度为1.0 mol/L计算)
开始沉淀的pH | 完全沉淀的pH | |
Fe3+ | 1.1 | 3.2 |
Fe2+ | 5.8 | 8.8 |
Zn2+ | 5.9 | 8.9 |
实验中可选用的试剂:30% H2O2、1.0 mol·L-1HNO3、1.0 mol·L-1 NaOH。
由除去铜的滤液制备ZnO的实验步骤依次为:①向滤液中加入30%的H2O2使其充分反应;
②滴加1.0 moL/L的氢氧化钠,调节pH约为_________________,使Fe3+沉淀完全;
③过滤;
④向滤液中滴加1.0 moL/L的氢氧化钠,调节pH约为________,使Zn2+沉淀完全;
⑤____________________________;
⑥900℃煅烧。
【答案】 Cu+H2O2+H2SO4=CuSO4+2H2O 加热(至沸) 淀粉溶液 蓝色褪去 偏高 5(或3.2≤pH<5.9) 10(或8.9≤pH≤11) 过滤、洗涤、干燥
【解析】废弃旧电池的铜帽加水超声洗涤去除表面的可溶性杂质,然后加入稀硫酸和双氧水,双氧水具有强氧化性,能在酸性条件下将铜氧化,最终生成铜盐,加入氢氧化钠降低酸性,然后加入足量的锌灰,由于锌的活泼性强于铜,故能把铜从其盐溶液中置换出来,剩余锌的化合物制备ZnO。
(1)①因为双氧水在酸性溶液中先把铜氧化成氧化铜,氧化铜又被稀硫酸溶解,生成硫酸铜,反应的化学方程式为:Cu+H2O2+H2SO4=CuSO4+2H2O;故答案为:Cu+H2O2+H2SO4=CuSO4+2H2O;
②过氧化氢性质比较稳定,若加热到153℃便猛烈的分解为水和氧气,将溶液中过量的H2O2除去可加热至沸,故答案为:加热至沸;
(2)①淀粉溶液为指示剂,当最后一滴Na2S2O3溶液滴入时,溶液蓝色褪去,半分钟颜色不变,说明滴定到达终点,故答案为:淀粉溶液;蓝色褪去并半分钟内不恢复;
②若留有H2O2,加入KI后,会有以下反应:H2O2+2I-+2H+=I2+2H2O,误当成2Cu2++4I-=2CuI(白色)↓+I2生成的碘,使测定结果偏高,故答案为:偏高;
(3)向滤液中加入30%H2O2,使其充分反应,目的使Fe2+转化完全为Fe3+,滴加NaOH溶液,调节溶液pH约为5(或3.2≤pH<5.9),使Fe3+沉淀完全,向滤液中滴加1.0molL-1NaOH,调节溶液pH约为10(或8.9≤pH≤11),使Zn2+沉淀完全,然后过滤、洗涤、干燥,在900℃煅烧,制得氧化锌,故答案为:5(或3.2≤pH<5.9) ;10(或8.9≤pH≤11);过滤、洗涤、干燥。


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案科目:高中化学 来源: 题型:
【题目】冶炼金属一般有下列四种方法:①焦炭法;②水煤气(H2或CO)法;③活泼金属置换法;④电解法.四种方法各有优缺点,在工业上均有应用.
(1)一种无色气体A与红热的炭反应,得到另一种无色气体B,B与灼热的氧化铜反应,又得到A,则A、B分别为(填序号).
A.O2、CO2
B.O2、CO
C.CO2、CO
D.CO、CO2
(2)下列说法错误的是(填序号).
A.对废旧金属最好的处理方法是回收、再利用
B.提炼金属要经过矿石的富集、冶炼、精炼三步
C.活泼金属的冶炼都是通过电解其盐溶液制得
D.热还原法中还原剂有焦炭、一氧化碳、氢气或活泼金属等
(3)钛(Ti)有“未来钢铁”之称,工业上常以TiCl4+2Mg ![]() Ti+2MgCl2获得海绵状钛,该反应在下列哪种环境中进行(填序号).
Ti+2MgCl2获得海绵状钛,该反应在下列哪种环境中进行(填序号).
A.稀有气体中
B.空气中
C.氮气中
D.CO2气体中.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R是短周期元素,原子序数依次增大.非金属X原子核外各层电子数之比为1:2,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨.请回答下列问题:
(1)元素X的最高价氧化物的电子式为;元素Z的离子结构示意图为 .
(2)单质铜和元素Y的最高价氧化物对应水化物的稀溶液发生反应的化学方程式为 .
(3)元素W位于周期表的第族,其非金属性比R弱,用原子结构的知识解释原因: .
(4)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液作该氧化物的吸收剂,写出吸收剂与足量该氧化物反应的离子方程式: .
(5)Y和Z组成的化合物ZY,被大量用于制造电子元件.工业上用Z的氧化物、X单质和Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为1:3,则该反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热条件下,硅单质和HCl反应生成SiHCl3是粗硅提纯的重要步骤.某小组设计如图所示装置完成上述转化(夹持装置略去). 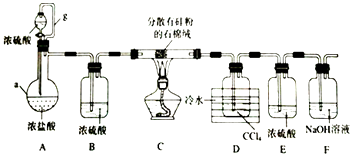
已知:SiHCl3的沸点为33.0°C,易溶于有机溶剂,能与水剧烈反应,在空气中易被氧化,CCl4的沸点为76.8°C.
请回答:
(1)仪器a的名称为;导管g的作用为;
(2)装置A中,浓硫酸体现的性质为;实验时,需先打开分液漏斗活塞,一段时间后,在点燃C处酒精灯,理由是;
(3)装置C中发生反应的化学方程式为;
(4)装置D中所得的液态混合物的分离方法为 . (填操作名称)
(5)反应后的气体通过装置F中的NaOH溶液后,对逸出气体的处理方法为;
(6)SiHCl3在潮湿的空气中被氧化,生成一种氧化物和一种无氧酸,该反应的化学方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甘草甜素在治疗丙肝、艾滋病、非典等疾病方面有一定疗效。甘草甜素在一定条件下可转化为甘草次酸。下列有关说法正确的是

A. 甘草甜素转化为甘草次酸属于酯的水解
B. 在Ni催化作用下,1mol 甘草次酸最多能与3molH2发生加成反应
C. 甘草甜素中含有羧基、羰基、碳碳双键、酚羟基等官能团
D. 甘草甜素、甘草次酸均可与Na2CO3、溴水等无机试剂发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甘草甜素在治疗丙肝、艾滋病、非典等疾病方面有一定疗效。甘草甜素在一定条件下可转化为甘草次酸。下列有关说法正确的是

A. 甘草甜素转化为甘草次酸属于酯的水解
B. 在Ni催化作用下,1mol 甘草次酸最多能与3molH2发生加成反应
C. 甘草甜素中含有羧基、羰基、碳碳双键、酚羟基等官能团
D. 甘草甜素、甘草次酸均可与Na2CO3、溴水等无机试剂发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用5%的H2O2溶液做了一个探究实验,实验步骤如下:步骤1:分别在2支大小相同的试管1和试管2中装入3.0mL5%的H2O2溶液.
步骤2:再分别往两支试管中滴入1~2滴1mol/LFeCl3溶液,
待试管中均有适量气泡出现时,将试管1放入盛有温度恒定为5℃冷水的烧杯中,试管2放入盛有温度恒定为40℃热水的烧杯中,同时用排水法收集产生的气体,并记录不同时刻(min)气体的总体积(mL),数据如下:
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | |
试管1 | 17.5 | 34.9 | 50.1 | 60.3 | 70.4 | 80.2 | 84.9 | 85.2 | 85.4 |
试管2 | 21.7 | 41.2 | 57.5 | 70.8 | 81.3 | 84.9 | 85.3 | 85.4 | 85.4 |
(1)向试管中加入的FeCl3溶液的作用 , 写出加入FeCl3溶液后发生的化学反应方程式:;
(2)相同时刻试管2中收集到的气体体积比试管1中多的原因是: , 由此该同学可以得出的实验结论是:;
(3)对比每分钟内收集到的气体体积变化,前5分钟内每分钟收集到的气体体积逐渐减小的原因是:;
(4)若用单位时间内收集到的气体体积表示反应的快慢,则2min到5min试管2中生成气体的速率为: . (请列出计算式并将计算结果保留3位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列叙述中不正确的是( )
A.NH4HSO4溶液中离子浓度大小关系:c(H+)>c(SO ![]() )>c(NH
)>c(NH ![]() )>c(OH﹣)
)>c(OH﹣)
B.等体积pH=a的醋酸与pH=b的NaOH溶液恰好中和,则a+b=14
C.Na2C2O4溶液中:c(OH﹣)=c(H+)+c(HC2O4﹣)+2c(H2C2O4)
D.NaHCO3溶液中:c(Na+)+c(H+)=c(HCO ![]() )+2c(CO
)+2c(CO ![]() )+c(OH﹣)
)+c(OH﹣)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com