
| A. |  四种基本反应类型与氧化还原反应的关系 | |
| B. | 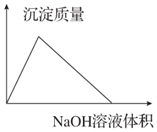 AlCl3溶液中滴加NaOH溶液生成沉淀的情况 | |
| C. |  Ba(OH)2溶液中滴加硝酸溶液导电性的情况 | |
| D. |  等体积等浓度稀硫酸分别与足量铁和镁反应的情况 |
分析 A.氧化还原反应的特征为有元素化合价的升降,置换反应一定属于氧化还原反应,复分解反应一定不属于氧化还原反应,有单质生成的分解反应属于氧化还原反应,有单质参加的化合反应属于氧化还原反应;
B.氯化铝溶液中加入氢氧化钠溶液先发生Al3++3OH-═Al(OH)3↓生成沉淀,后发生Al(OH)3+NaOH═NaAlO2+2H2O沉淀溶解至最后消失,结合方程式判断前后消耗氢氧化钠溶液体积关系;
C.硝酸和氢氧化钡的反应方程式为2HNO3+Ba(OH)2=Ba(NO3)2+2H2O,随着硝酸的加入,溶液体积增大,则离子的浓度逐渐减小,但不可能为0,导电性也也减弱;
D.等体积等浓度稀硫酸分别与足量铁和镁反应,生成氢气的体积相等,Mg与硫酸反应速率较快.
解答 解:A、复分解反应一定不属于氧化还原反应,则不会出现交叉,置换反应一定属于氧化还原反应,则应为包含,部分的化合与分解反应属于氧化还原反应,则不能是包含,应为交叉关系,故A正确;
B.氯化铝溶液中加入氢氧化钠溶液先发生Al3++3OH-═Al(OH)3↓生成沉淀,后发生Al(OH)3+NaOH═NaAlO2+2H2O沉淀溶解至最后消失,由方程式可知,前后NaOH溶液体积之比为3:1,故其图象为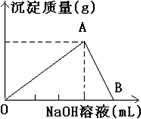 ,故B错误;
,故B错误;
C.硝酸和氢氧化钡的反应方程式为2HNO3+Ba(OH)2=Ba(NO3)2+2H2O,随着硝酸的加入,溶液体积增大,则离子的浓度逐渐减小,但不可能为0,导电性也也减弱,图象与实际不相符,故C错误;
D.等体积等浓度稀硫酸分别与足量铁和镁反应,硫酸完全反应,生成氢气的体积相等,Mg与硫酸反应速率较快,图象与实际不相符,故D错误,
故选A.
点评 本题是图象解析题,分析图象时要注意曲线的“原点”、“转折点”等的意义,对“数据”、“形状”、“含义”、“性质”进行综合思考,从中发掘隐含信息快速解题,侧重对学生综合能力的考查.


科目:高中化学 来源: 题型:选择题
| A. | NaHSO4和Ba(OH)2 | B. | AlCl3和NaOH | C. | NaAlO2和H2SO4 | D. | Na2CO3和HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2S?2H++S2- | B. | H2S+H2O?H3O++HS- | ||
| C. | HCl?H++Cl- | D. | HClO═H++ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ | |
| B. | 氧化亚铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O | |
| C. | NH4HCO3溶液与足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H2O | |
| D. | AlCl3溶液中加入足量的氨水:Al3++4OH-═AlO2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述反应中氧化剂和还原剂的物质的量之比为5:6 | |
| B. | 产生白色烟雾的原因是生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成酸滴(雾) | |
| C. | 上述反应中消耗3molP时,转移电子的物质的量为15mol | |
| D. | 产物P2O5为酸性氧化物,但不是磷酸的酸酐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 电子从Zn极流出,流入Fe极,经盐桥回到Zn极 | |
| B. | 烧杯b中发生的电极反应为Zn-2e-═Zn2+ | |
| C. | 烧杯a中发生反应O2+4H++4e-═2H2O,溶液pH降低 | |
| D. | 向烧杯a中加入少量KSCN溶液,则溶液会变成红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3$→_{催化剂}^{O_{2}}$NO$\stackrel{NaOH溶液}{→}$NaNO3 | |
| B. | Fe2O3$→_{高温}^{Al}$Fe$→_{点燃}^{Cl_{2}}$FeCl3 | |
| C. | SiO2$→_{△}^{H_{2}O}$H2SiO3$\stackrel{NaOH溶液}{→}$NaSiO3 | |
| D. | NaSO4溶液$\stackrel{BaCl_{2}溶液}{→}$BaSO4$\stackrel{盐酸}{→}$BaCl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com