
(1)实验室用氯化铵固体制取氨气的化学方程式是________.
(2)将4.48 L(标准状况)氨气通入水中得到0.05 L溶液,所得溶液的物质的量浓度是________.
(3)现有100 mL AlCl3与MgSO4的混合溶液,分成两等份.
①向其中一份中加入10 mL 4 mol/L的氨水,恰好完全反应,其中AlCl3与氨水反应的离子方程式是________.继续加入1 mol/L NaOH溶液至10 mL时,沉淀不再减少,沉淀减少的离子方程式是________,减少的沉淀的物质的量是________.
②向另一份中加入a mL 1 mol/L BaCl2溶液能使SO42-沉淀完全,a=________.
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
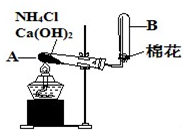 如图是实验室用氯化铵和熟石灰制取氨气的实验装置图.请回答以下各问题:
如图是实验室用氯化铵和熟石灰制取氨气的实验装置图.请回答以下各问题:查看答案和解析>>
科目:高中化学 来源:浙江省东阳中学2012届高三上学期期中考试化学试题 题型:058
某校化学学习小组拟验证NO能被氨气还原并测定其转化率,设计如下实验:
参考知识:NO气体与FeSO4溶液反应生成可溶性硫酸亚硝基合铁(Ⅱ):NO+FeSO4=Fe(NO)SO4

试回答下列问题:
(1)实验室用氯化铵与氢氧化钙固体制备氨气,应选用的装置是________

该反应的化学方程式________
实验室通常用________法收集氨气,检验该气体是否收集满方法________
(2)装置③、④若用同一装置,则该装置中所盛装的药品是________
A.Na2O2
B.浓硫酸
C.P2O5
D.碱石灰
(3)装置⑥中,粗玻璃管X的作用________,装置⑦的作用________
(4)装置⑥的广口瓶中,除生成Fe(NO)SO4外,还有白色沉淀生成,写出生成该沉淀的离子方程式________
(5)若参加反应的NO为2.688 L(标准状况,下同),氨气过量,最后收集到2.016 L N2,则装置⑤中NO的转化率为________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com