
| A、CH4 |
| B、NH3 |
| C、H2O |
| D、CO2 |
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| T | M层的电子数为K层电子数的3倍 |
| X | 其氢化物的空间构型为正四面体 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纯锌与稀硫酸反应 |
| B、纯锌与浓硫酸反应 |
| C、粗锌(含铅.铜杂质)与浓硝酸反应 |
| D、粗锌(含铅.铜杂质)与稀硫酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:

A、 、HCHO和 、HCHO和  |
B、 、CH3OH和 、CH3OH和  |
C、 、HCHO和 、HCHO和  |
D、 、CH3CHO和 、CH3CHO和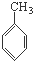 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 硫铁矿又称黄铁矿,是生产硫酸的原料,其主要成分为FeS2.850℃~950℃时,硫铁矿在空气中煅烧,可能发生下列反应(设空气中N2与O2体积比为4:1):
硫铁矿又称黄铁矿,是生产硫酸的原料,其主要成分为FeS2.850℃~950℃时,硫铁矿在空气中煅烧,可能发生下列反应(设空气中N2与O2体积比为4:1):查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X:3s23p1 Y:3s23p5 |
| B、X:2s22p3 Y:2s22p5 |
| C、X:3s23p1 Y:3s23p4 |
| D、X:3s2 Y:2s22p3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com