
分析 (1)电子层数越多半径大,电子层相同时核电荷数越小,半径越大;单质广泛用作半导体材料的是硅;
(2)铝是13号元素,三个电子层,最外层三个电子;氧化铝是两性氧化物,可与强酸强碱反应,所以可溶于氢氧化钠;
(3)电解法:冶炼活泼金属(K、Ca、Na、Mg、Al),一般用电解熔融的氯化物(Al是电解熔融的三氧化二铝)制得;
(4)Al与氧化铁在高温下反应生成氧化铝与Fe,该反应为铝热反应,放出大量的热.
解答 解:(1)电子层数越多半径大,电子层相同时核电荷数越小,半径越大,所以在钠、铝、碳、硅的半径大小为:钠、铝、硅、碳;单质广泛用作半导体材料的是硅,故答案为:Na;Si;
(2)铝是13号元素,三个电子层,最外层三个电子,所以铝在周期表中位于第三周期第IIIA族,;氧化铝是两性氧化物,可与强酸强碱反应,所以可溶于氢氧化钠,反应的方程式为:Al2O3+2OH-=2AlO2-+H2O,故答案为:三;IIIA;Al2O3+2OH-=2AlO2-+H2O;
(3)电解法:冶炼活泼金属(K、Ca、Na、Mg、Al),一般用电解熔融的氯化物(Al是电解熔融的三氧化二铝)制得,所以MgCl2和NaCl用电解制得,故选BC;
(4)Al与氧化铁在高温下反应生成氧化铝与Fe,反应方程式为:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe,该反应为铝热反应,放出大量的热,属于放热反应,
故答案为:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe.
点评 本题考查元素周期表和金属的冶炼,题目难度不大,注意根据金属的活泼性确定金属的冶炼方法.注意铝是活泼金属,采用电解法冶炼.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
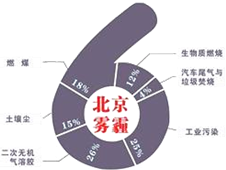 中科院大气研究所研究员张仁健课题组与同行合作,对北京地区PM2.5有6个重要来源,其中,汽车尾气和燃煤分别占4%、18%.用于净化汽车尾气的反应为2NO(g)+2CO(g)$\stackrel{催化剂}{?}$ 2CO2(g)+N2(g),已知该反应在570K时平衡常数为1×1059,但反应很慢.下列说法正确的是( )
中科院大气研究所研究员张仁健课题组与同行合作,对北京地区PM2.5有6个重要来源,其中,汽车尾气和燃煤分别占4%、18%.用于净化汽车尾气的反应为2NO(g)+2CO(g)$\stackrel{催化剂}{?}$ 2CO2(g)+N2(g),已知该反应在570K时平衡常数为1×1059,但反应很慢.下列说法正确的是( )| A. | 装有尾气净化装置的汽车排出的气体中不再含有NO或CO | |
| B. | 提高尾气净化效率的常用方法是升高温度 | |
| C. | 增大压强,上述平衡右移,故实际操作中可通过增压的方式提高其净化效率 | |
| D. | 提高尾气净化效率的最佳途径是使用高效催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉 | B. | 蔗糖 | C. | 果糖 | D. | 麦芽糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H$\underset{\stackrel{\;}{C}}{•}$$\underset{\stackrel{\;}{l}}{•}$ | B. | $\underset{\stackrel{\;}{F}}{•}$$\underset{\stackrel{\;}{e}}{•}$Cl2 | C. | K$\underset{\stackrel{\;}{M}}{•}$$\underset{\stackrel{\;}{n}}{•}$O4 | D. | Na2$\underset{\stackrel{\;}{S}}{•}$O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化钠溶液在电流作用下电离成钠离子和氯离子. | |
| B. | 硫酸钡难溶于水,但硫酸钡是电解质 | |
| C. | 溶于水后电离出氢离子的化合物都是酸 | |
| D. | 二氧化碳的水溶液能导电,故二氧化碳属于电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,它的化学键属于共价键;含有离子键和共价键的化合物的化学式为Na2O2.
,它的化学键属于共价键;含有离子键和共价键的化合物的化学式为Na2O2.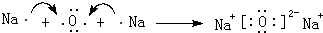 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com