
【题目】氯化镁晶体具有如下转化关系:

下列说法错误的是
A.固体I可溶于饱和NH4Cl溶液
B.气体I能使无水CuSO4变蓝色
C.溶液I和溶液Ⅱ常温下均能与Cu反应
D.在固体Ⅱ的浊液中加入KI溶液可产生黄色沉淀
科目:高中化学 来源: 题型:
【题目】下列文字表述与反应的离子方程式对应且正确的是 ( )
A. 溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+=AgBr↓
B. 用醋酸除去水垢:CaCO3 + 2H+=Ca2+ + H2O + CO2↑
C. 苯酚与纯碱溶液混合:2C6H5OH + CO32- ![]() CO2 ↑+ H2O + 2C6H5O-
CO2 ↑+ H2O + 2C6H5O-
D. 甲醛溶液与足量的银氨溶液共热:HCHO+4Ag(NH3)2++4OH-![]() CO32-+2NH4++4Ag↓+6NH3+2H2O
CO32-+2NH4++4Ag↓+6NH3+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷既是重要的能源也是重要的化工原料。
已知反应CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g),起始时向体积为V的恒容密闭容器中通入2molCH4和3molNO2,测得CH4、N2、H2O的物质的量浓度与时间的关系如图所示。
N2(g)+CO2(g)+2H2O(g),起始时向体积为V的恒容密闭容器中通入2molCH4和3molNO2,测得CH4、N2、H2O的物质的量浓度与时间的关系如图所示。
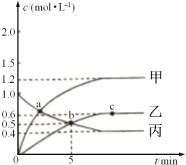
(1)容器体积V=_____L。
(2)图中表示H2O的物质的量浓度与时间关系的是曲线_____(填“甲”“乙"或"丙")。
(3)0~5min内,用N2表示的化学反应速率为_____mol·L-1·min-1。
(4)a、b、c三点中达到平衡的点是______。达到平衡时,NO2的转化率是_____。(物质平衡转化率=转化的物质的量/起始的物质的量×100%)。
(5)a点时,n(CH4):n(NO2)=_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,800 ℃时A、B、C三种气体在密闭容器中反应时浓度的变化,只从图上分析不能得出的结论是
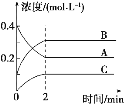
A. 发生的反应可表示为2A(g)![]() 2B(g)+C(g)
2B(g)+C(g)
B. 前2 min A的分解速率为0.1 mol/(L·min)
C. 开始时,正、逆反应同时开始
D. 2 min时,A、B、C的浓度之比为2∶3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,A、B、C三种气体在恒容密闭容器中进行反应,反应从0~2min进行过程中,在不同反应时间各物质的量的变化情况如图所示。
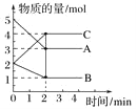
(1)该反应的反应物是____________,生成物是________。
(2)化学方程式为___________________________________________。
(3)能否计算反应开始至2min时,用C表示的反应速率?________,若不能,则其原因是_________________________________________________。
(4)关于该反应的说法正确的是________(填字母,下同)。
a.到达2min时,反应停止
b.在2min之前A的消耗速率大于A的生成速率
c.在2min时达到平衡状态是因为此时反应物总物质的量与生成物总物质的量相等
d.2min时正反应速率与逆反应速率相等
(5)下列可判断反应已达到平衡状态的是________。
a.A、B、C的反应速率相等
b.A、B的反应速率之比为2∶1
c.混合气体的压强不变
d.生成1molC的同时消耗1molA和0.5molB
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环之间共用一个碳原子的化合物称为螺环化合物,螺[2,2]戊烷(![]() )是最简单的一种。下列关于该化合物的说法不正确的是
)是最简单的一种。下列关于该化合物的说法不正确的是
A. 与环戊烯互为同分异构体
B. 二氯代物超过四种(不考虑空间异构)
C. 所有碳原子均处同一平面
D. 由该物质生成1 mol C5H12需要2 mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PET俗称涤纶树脂,是一种热塑性聚酯;PMMA俗称有机玻璃。工业上以基础化工原料合成这两种高分子材料的路线如下:
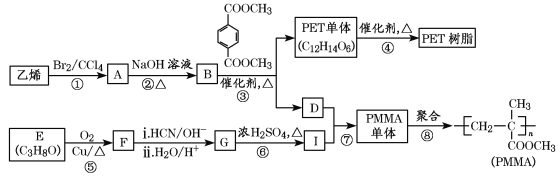
已知:Ⅰ.RCOOR′+R″OH![]() RCOOR″+R′OH(R、R′、R″代表烃基)
RCOOR″+R′OH(R、R′、R″代表烃基)
II、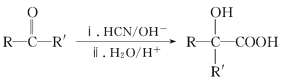 (R、R′、代表烃基)
(R、R′、代表烃基)
(1)指出下列反应的反应类型:反应③_________;反应⑥______。
(2)B的名称为_______;
反应②的化学方程式为____________________________。
反应⑤的化学方程式为____________________________。
(3)PET单体(C12H14O6)的结构简式为_______。
(4)下列说法正确的是________(填字母)。
a.B和D互为同系物
b.⑧为加聚反应
c.F和丙醛互为同分异构体
d.G能发生加成反应和酯化反应
(5)I的同分异构体中,满足下列条件的有___________种。(不包括I)
①能与NaOH溶液反应;②含有碳碳双键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图,下列关于该有机物的说法正确的是
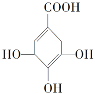
A.分子式为C7H6O5
B.分子中含有两种官能团
C.该物质能发生加成反应,氧化反应和取代反应
D.在水溶液中羧基和羟基均能电离出H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.实验室选用酸性KMnO4溶液与H2C2O4溶液反应来探究影响化学反应速率的因素:
实验前先用酸性KMnO4标准溶液滴定未知浓度的草酸
(1)配平反应原理离子方程式:
___MnO4-+ __H2C2O4+___→___Mn2++ ___CO2↑+____H2O
(2)探究影响化学反应速率的因素
实验 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度 | ||
浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | ||
① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
a.探究温度对化学反应速率影响的实验编号是_______(填编号,下同),探究反应物浓度对化学反应速率影响的实验编号是_______。
b.混合液褪色时间由大到小的顺序是_____________。
c.测得某次实验(恒温)时溶液中Mn2+物质的量与时间关系如图所示,请解释“n(Mn2+)在反应起始时变化不大,一段时间后快速增大”的主要原因:_______。

Ⅱ. 用酸性KMnO4溶液滴定含杂质的Na2C2O4样品(已知杂质不与KMnO4和H2SO4溶液反应)。
实验步骤:准确取1 g Na2C2O4样品,配成
(3)高锰酸钾溶液应装在____滴定管中。(填“酸式”或“碱式”)
(4)滴定至终点时的实验现象是:_________。
(5)计算样品中Na2C2O4的纯度是______%。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com