
在FeCl3和CuCl2的混合溶液中加入铁屑,反应结束后滤出固体物质,滤液中的阳离子可能是 ( )
①只有Fe2+ ②Fe2+和Fe3+
③Fe2+和Cu2+ ④Cu2+和Fe3+
A.①③ B.②④ C.①④  D.②③
D.②③
科目:高中化学 来源: 题型:
目前世界上60%的镁是从海水提取的。海水提镁的主要流程如下:
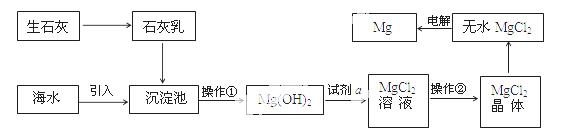
提示:  ①MgCl2晶体的化学式为MgCl2•6H2O;
①MgCl2晶体的化学式为MgCl2•6H2O;
②MgO的熔点为2852℃,无水MgCl2的熔点为714℃。
(1)操作①的名称是 , 操作②的名称 、 、过滤。
(2)试剂a的名称是 。
(3)用氯化镁电解生产金属镁的化学方程式为: 。
(4)工业上是将氢氧化镁转变为氯化镁,再电解氯化镁来制取镁单质;而不采用:加热Mg(OH)2得到MgO,再电解熔融MgO的 方法制金属镁,其原因是 。
方法制金属镁,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
用铝箔包裹0.1 mol金属钠,用针扎出一些小孔,放入水中,完全反应后用排水集气法收集产生的气体,则收集到的气体为(标准状况)( )
A.O2和H2的混合气体 B.1.12  L H2
L H2
C.大于1.12 L H2 D.小于1.12 L H2
查看答案和解析>>
科目:高中化学 来源: 题型:
完成下面有关钠、镁、铝的计算及判断。
(1)取w g钠、镁、铝分别与足量盐酸反应,在相同条件下产生氢气的体积之比是________。
(2)取0.1 mol钠、镁、铝分别与足量盐酸反应,在相同条件下产生氢气的体积之比是________。
(3)若产生相同体积(同温同压)的氢气,所需钠、镁、铝三种金属的物质的量之比是________;质量之比是________。
(4)若将0.2 mol钠、镁、铝分别投入10 mL 1 mol·L-1盐酸中,在标准状况下产生氢气体积的大小顺序是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
20 g由两种金属粉末组成的混合物,与足量的盐酸充分反应后得到11.2 L氢气(标
准状况),这种金属混合物的组成可能是 ( )
A.Mg和Al B.Al和Fe
C.Fe和Zn D.Zn和Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
用一定量的铁与足量的稀H2SO4及足量的CuO制成单质铜,有人设计以下两种方案:①Fe H2
H2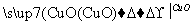 Cu ②CuO
Cu ②CuO CuSO4
CuSO4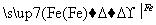 Cu
Cu
若按实验原则进行操作,则两者制得单质铜的量的比较中,正确的是 ( )
A.①多 B.②多
C.相等 D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸亚铁可与等物质的量的硫酸铵生成硫酸亚铁铵:(NH4)2SO4·FeSO4·6H2O,商品名称为莫尔盐,是一种复盐。一般亚铁盐在空气中易被氧气氧化,形成复盐后就比较稳定。与其他复盐一样,硫酸亚铁铵在水中的溶解度比组成它的每一种盐的溶解度都小,且几乎不溶于乙醇,利用这一性质可以制取硫酸亚铁铵晶体。三种盐的溶解度(单位为g/l00gH2O)见下表:
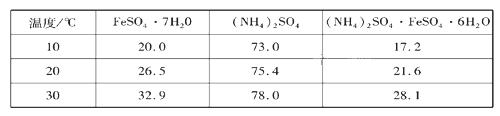
实验用品: Fe屑(含少量碳)、3mol/LH2SO4、( NH4)2SO4、蒸馏水、无水乙醇。
实验步骤流程图:
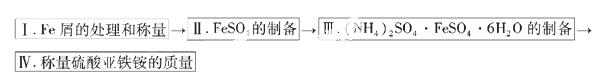
请完成以下实验记录:
(1)步骤I中用10% Na2CO3的热溶液处理铁屑的目的是 ,经处理后的干燥铁屑质量记为m1;
(2)将称量好的Fe屑放入锥形瓶中, 加入适量3mol/LH2SO4溶液,放在水浴中加热至气泡量产生较少时为止(有氢气生成,用明火加热注意安全)。趁热过滤,并用少量热水洗涤锥形瓶及滤纸,将滤液和洗涤液一起转移至蒸发皿中。将滤纸上的固体常温干燥后称重,记为m2;
加入适量3mol/LH2SO4溶液,放在水浴中加热至气泡量产生较少时为止(有氢气生成,用明火加热注意安全)。趁热过滤,并用少量热水洗涤锥形瓶及滤纸,将滤液和洗涤液一起转移至蒸发皿中。将滤纸上的固体常温干燥后称重,记为m2;
(3)称取一定质量的(NH4)2SO4,加入______ g(用含m1和m2的代数式表示,要求化简,下同。)水配制成室温下(20℃)的饱和溶液,并将其加入到上面实验的蒸发皿中,缓缓加热,浓缩至表面出现结晶薄膜为止。放置冷却,得到硫酸亚铁铵的晶体,过滤后用____________洗涤晶体。
(4)产品纯度的测定
先称取产品1.600g,加水溶解,配成100ml溶液,移取25.00mL待测溶液与锥形瓶中,再用硫酸酸化的0.0100mol/LKMnO4标准溶液进行滴定其中的Fe2+,达到滴定终点时消耗标准液的平均值为20.00mL,则样品中的(NH4)2SO4·FeSO4·6H2O的质量分数?(列式计算)
查看答案和解析>>
科目:高中化学 来源: 题型:
原子序数依次增大的X、Y、Z、W四种短周期元素,X、W原子的最外层电子数与其电子层数相等,X、Z的最外层电子数之和与Y、W的最外层
电子数之和相等。甲的化学式为YX3,是一种刺激性气味的气体,乙是由X、Y、Z组成的盐。下列说法正
确的是 ( )
A.原子半径:W>Y>Z,简单离子半径: Y>Z>W
B.YX 3的空间构型是三角锥型,而Y2X4的空间构型类似于乙烯的空间构型
C.测得乙的水溶液呈酸性,则溶液中乙盐阳离子浓度大于酸根离子浓度
D. W的氯化物熔点低,易升华,但水溶液能导电,由此推断它属于弱电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
氰气:(CN)2,结构:N≡C-C≡N;化学性质与卤素单质相似,下列叙述中正确的是
A.(CN)2分子中C—C键的键长小于F—F键的键长
B.氰化钠和氰化银均不溶于水
C.(CN)2不可以和不饱和烃起加成反应
D.(CN)2和NaOH溶液反应可生成NaCN、NaOCN和H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com