
| A、④⑤③ | B、⑥①⑤③ |
| C、⑧① | D、⑥②⑤③ |


科目:高中化学 来源: 题型:
| ||
| 催化剂 |
| 容器 | 甲 | 乙 | 丙 |
| 起始物质投入量 | 3molH2、2molN2 | 6molH2、4molN2 | 、2molNH3 |
| 达到平衡的时间 /min | t | 5 | 8 |
| 平衡时N的浓度/mol.L-1 | c1 | 3 | |
| N的体积分数 | ω1 | ω2 | ω3 |
| 混合气体密度/g.L-1 | ρ1 | ρ2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 根据氧化还原反应:2Ag++Cu═Cu2++2Ag设计的原电池如图所示,其中盐桥内装琼脂饱和KNO3溶液.
根据氧化还原反应:2Ag++Cu═Cu2++2Ag设计的原电池如图所示,其中盐桥内装琼脂饱和KNO3溶液.查看答案和解析>>
科目:高中化学 来源: 题型:
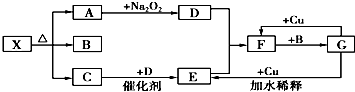
查看答案和解析>>
科目:高中化学 来源: 题型:
 )
)| 选项 | 气体 | 试剂 | 现象 | 结论 |
| A | SO2 | 酸性KMnO4溶液 | 溶液褪色 | SO2有氧化性 |
| B | C2H4 | 溴水 | 溶液褪色 | 能发生加成反应 |
| C | X | 澄清石灰水 | 溶液变浑浊 | X不一定是CO2 |
| D | Cl2 | 紫色石蕊试液 | 溶液先变红后褪色 | Cl2有酸性和漂白性 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向0.1 mol?L-1NH4 Cl溶液中通入大量氨气:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| B、0.1 mol?L-1的醋酸与0.01 mol?L-1的醋酸相比,前者[H+]大于后者[H+]的10倍 |
| C、已知Ka(HF)=7.2×10-4,Ka(HCN)=4.9×10-10,等体积等浓度的NaF、NaCN溶液中,前者离子总数小于后者 |
| D、NaB溶液的pH=8,c(Na+)-c(B-)=9.9×10-7 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 反应先后顺序 |
| A | 含Fe3+、Cu2+、H+的溶液中加入锌粉 | Cu 2+、Fe3+、H+ |
| B | 含I-、S2-、Br-的溶液中不断通入氯气 | S2-、I-、Br- |
| C | 含Cl-、Br-、I-的溶液中逐滴加入AgNO3溶液 | Cl-、Br-、I- |
| D | 含Al 3+、H+、NH4+的溶液中逐滴加入NaOH溶液 | H+、NH4+、Al 3+ |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com