
ЎҫМвДҝЎҝөӘФӘЛШөД»ҜәПОпЦЦАа·ұ¶аЈ¬РФЦКТІёчІ»ПаН¬ЎЈЗл»ШҙрПВБРОКМвЈә
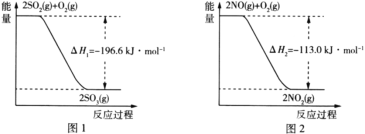
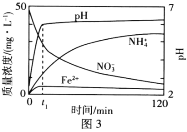
ЈЁ1Ј©NO2УРҪПЗҝөДСх»ҜРФЈ¬ДЬҪ«SO2Сх»ҜіЙSO3Ј¬ЧФЙнұ»»№ФӯОӘNOЈ¬ТСЦӘПВБРБҪ·ҙУҰ№эіМЦРДЬБҝұд»ҜИзНј1ЎўНј2ЛщКҫЈ¬ФтNO2Сх»ҜSO2ЙъіЙSO3(g)өДИИ»ҜС§·ҪіМКҪОӘ____ЎЈ
ЈЁ2Ј©ФЪөӘЖшұЈ»ӨПВЈ¬ФЪКөСйКТЦРУГЧгБҝөДFe·Ы»№ФӯKNO3ИЬТәЈЁpH =2.5Ј©ЎЈ·ҙУҰ№эіМЦРИЬТәЦРПа№ШАлЧУөДЦКБҝЕЁ¶ИЎўpHЛжКұјдөДұд»ҜЗъПЯЈЁІҝ·Цёұ·ҙУҰІъОпЗъПЯВФИҘЈ©ИзНј3ЛщКҫЎЈЗлёщҫЭНј3ЦРРЕПўРҙіц![]() minЗ°·ҙУҰөДАлЧУ·ҪіМКҪ____ЎЈ
minЗ°·ҙУҰөДАлЧУ·ҪіМКҪ____ЎЈ
ЈЁ3Ј©СРҫҝИЛФұУГ»оРФМҝ¶ФЖыіөОІЖшЦРөДNOҪшРРОьёҪЈ¬·ўЙъ·ҙУҰC(s) +2NO(g)![]() N2(g) +CO2(g)
N2(g) +CO2(g) ![]() H<0ЎЈФЪәгС№ГЬұХИЭЖчЦРјУИлЧгБҝөД»оРФМҝәНТ»¶ЁБҝөДNOЖшМеЈ¬·ҙУҰПаН¬КұјдКұЈ¬ІвөГNOөДЧӘ»ҜВК
H<0ЎЈФЪәгС№ГЬұХИЭЖчЦРјУИлЧгБҝөД»оРФМҝәНТ»¶ЁБҝөДNOЖшМеЈ¬·ҙУҰПаН¬КұјдКұЈ¬ІвөГNOөДЧӘ»ҜВК![]() (NO)ЛжОВ¶ИөДұд»ҜИзНј4ЛщКҫЈә
(NO)ЛжОВ¶ИөДұд»ҜИзНј4ЛщКҫЈә
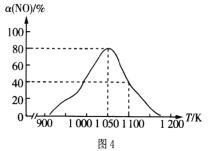
ўЩУЙНј4ҝЙЦӘЈ¬ОВ¶ИөНУЪ1 050 KКұЈ¬NOөДЧӘ»ҜВКЛжОВ¶ИЙэёЯ¶шФцҙуЈ¬ФӯТтКЗ__Ј»ОВ¶ИОӘ1050 KКұCO2өДЖҪәвМе»э·ЦКэОӘ__ЎЈ
ўЪ¶ФУЪ·ҙУҰC(s) +2NO(g)![]() N2(g)+CO2(g)өД·ҙУҰМеПөЈ¬ұкЧјЖҪәвіЈКэ
N2(g)+CO2(g)өД·ҙУҰМеПөЈ¬ұкЧјЖҪәвіЈКэ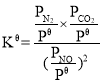 Ј¬ЖдЦР
Ј¬ЖдЦР![]() ОӘұкЧјС№ЗҝЈЁ1ЎБ105PaЈ©Ј¬
ОӘұкЧјС№ЗҝЈЁ1ЎБ105PaЈ©Ј¬![]() Ўў
Ўў![]() әН
әН![]() ОӘёчЧй·ЦөДЖҪәв·ЦС№Ј¬Из
ОӘёчЧй·ЦөДЖҪәв·ЦС№Ј¬Из![]() =
=![]() ЎӨ
ЎӨ![]() Ј¬
Ј¬![]() ОӘЖҪәвЧЬС№Ј¬
ОӘЖҪәвЧЬС№Ј¬![]() ОӘЖҪәвПөНіЦР NOөДОпЦКөДБҝ·ЦКэЎЈИфNOөДЖрКјОпЦКөДБҝОӘ1 molЈ¬јЩЙи·ҙУҰФЪәг¶ЁОВ¶ИәНұкЧјС№ЗҝПВҪшРРЈ¬NOөДЖҪәвЧӘ»ҜВКОӘ
ОӘЖҪәвПөНіЦР NOөДОпЦКөДБҝ·ЦКэЎЈИфNOөДЖрКјОпЦКөДБҝОӘ1 molЈ¬јЩЙи·ҙУҰФЪәг¶ЁОВ¶ИәНұкЧјС№ЗҝПВҪшРРЈ¬NOөДЖҪәвЧӘ»ҜВКОӘ![]() Ј¬Фт
Ј¬Фт![]() =__ЈЁУГә¬
=__ЈЁУГә¬![]() өДЧојтКҪұнКҫЈ©ЎЈ
өДЧојтКҪұнКҫЈ©ЎЈ
ЈЁ4Ј©АыУГПЦҙъКЦіЦјјКхҙ«ёРЖчМҪҫҝС№Зҝ¶Ф2NO2 (g)![]() N2O4(g)ЖҪәвТЖ¶ҜөДУ°ПмЎЈФЪәг¶ЁОВ¶ИәНұкЧјС№ЗҝМхјюПВЈ¬НщХлНІЦРідИлТ»¶ЁМе»эөДNO2ЖшМеәуГЬ·вІўұЈіЦ»оИыО»ЦГІ»ұдЎЈ·ЦұрФЪ
N2O4(g)ЖҪәвТЖ¶ҜөДУ°ПмЎЈФЪәг¶ЁОВ¶ИәНұкЧјС№ЗҝМхјюПВЈ¬НщХлНІЦРідИлТ»¶ЁМе»эөДNO2ЖшМеәуГЬ·вІўұЈіЦ»оИыО»ЦГІ»ұдЎЈ·ЦұрФЪ![]() sЎў
sЎў![]() sКұСёЛЩТЖ¶Ҝ»оИыәуІўұЈіЦ»оИыО»ЦГІ»ұдЈ¬Ів¶ЁХлНІДЪЖшМеС№Зҝұд»ҜИзНј5ЛщКҫЎЈ
sКұСёЛЩТЖ¶Ҝ»оИыәуІўұЈіЦ»оИыО»ЦГІ»ұдЈ¬Ів¶ЁХлНІДЪЖшМеС№Зҝұд»ҜИзНј5ЛщКҫЎЈ
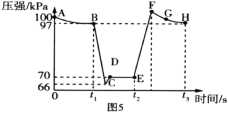
ўЩBЎўEБҪөг¶ФУҰөДХэ·ҙУҰЛЩВКҙуРЎОӘ![]() __ЈЁМоЎ° > ЎұЎ° < Ўұ»тЎ° =ЎұЈ©
__ЈЁМоЎ° > ЎұЎ° < Ўұ»тЎ° =ЎұЈ©![]() ЎЈ
ЎЈ
ўЪEЎўFЎўGЎўHЛДөг¶ФУҰЖшМеөДЖҪҫщПа¶Ф·ЦЧУЦКБҝЧоҙуөДөгОӘ__ЎЈ
Ўҫҙр°ёЎҝNO2(g)Ј«SO2(g)=SO3(g)Ј«NO(g) ЎчH=Јӯ41.8kJЎӨmolЈӯ1 4FeЈ«NO3ЈӯЈ«10HЈ«=4Fe2Ј«Ј«NH4Ј«Ј«3H2O ОВ¶ИөНУЪ1050KКұЈ¬·ҙУҰОҙҙпөҪЖҪәвЧҙМ¬Ј¬ЛжОВ¶ИЙэёЯЈ¬·ҙУҰЛЩВКјУҝмЈ¬NOЧӘ»ҜВКФцҙу 40% ![]() > H
> H
ЎҫҪвОцЎҝ
(1)ёщҫЭНј1әННј2ЦРөДРЕПўЈ¬ҝЙөГИИ»ҜС§·ҪіМКҪўЩ2SO2(g)Ј«O2(g)![]() 2SO3(g) ЎчH1=Јӯ196.6kJЎӨmolЈӯ1Ј¬ўЪ2NO(g)Ј«O2(g)
2SO3(g) ЎчH1=Јӯ196.6kJЎӨmolЈӯ1Ј¬ўЪ2NO(g)Ј«O2(g)![]() 2NO2(g) ЎчH2=Јӯ113.0kJЎӨmolЈӯ1Ј¬
2NO2(g) ЎчH2=Јӯ113.0kJЎӨmolЈӯ1Ј¬![]() (·ҙУҰўЩЈӯ·ҙУҰўЪ)ҝЙөГNO2Сх»ҜSO2өД·ҙУҰ·ҪіМКҪЈ¬NO2(g)Ј«SO2(g)=NO(g)Ј«SO3(g) ЎчH=
(·ҙУҰўЩЈӯ·ҙУҰўЪ)ҝЙөГNO2Сх»ҜSO2өД·ҙУҰ·ҪіМКҪЈ¬NO2(g)Ј«SO2(g)=NO(g)Ј«SO3(g) ЎчH=![]() (ЎчH1ЈӯЎчH2)=
(ЎчH1ЈӯЎчH2)=![]() [Јӯ196.6kJЎӨmolЈӯ1Јӯ(Јӯ113.0kJЎӨmolЈӯ1)]=Јӯ41.8kJЎӨmolЈӯ1Ј¬ФтNO2Сх»ҜSO2ЙъіЙSO3(g)өДИИ»ҜС§·ҪіМКҪОӘNO2(g)Ј«SO2(g)=SO3(g)Ј«NO(g)ЎчH=Јӯ41.8kJЎӨmolЈӯ1Ј»
[Јӯ196.6kJЎӨmolЈӯ1Јӯ(Јӯ113.0kJЎӨmolЈӯ1)]=Јӯ41.8kJЎӨmolЈӯ1Ј¬ФтNO2Сх»ҜSO2ЙъіЙSO3(g)өДИИ»ҜС§·ҪіМКҪОӘNO2(g)Ј«SO2(g)=SO3(g)Ј«NO(g)ЎчH=Јӯ41.8kJЎӨmolЈӯ1Ј»
(2)ёщҫЭНјПсЈ¬t1minЗ°Ј¬ИЬТәОӘЛбРФЈ¬·ҙУҰәуpHҝмЛЩФцҙуЈ¬NO3ЈӯөДБҝФЪјхРЎЈ¬¶шFe2Ј«әНNH4Ј«өДБҝФЪФцјУЈ¬ЛөГчFeәНNO3Јӯ·ҙУҰЙъіЙFe2Ј«әНNH4Ј«Ј¬АлЧУ·ҪіМКҪОӘ4FeЈ«NO3ЈӯЈ«10HЈ«=4Fe2Ј«Ј«NH4Ј«Ј«3H2OЈ»
(3)ўЩОВ¶ИөНУЪ1050KКұЈ¬ОВ¶ИҪПөНЈ¬»ҜС§·ҙУҰЛЩВКҪПВэЈ¬·ҙУҰГ»УРҙпөҪЖҪәвЈ¬ЖҪәвПтХэ·ҙУҰ·ҙУҰТЖ¶ҜЈ¬ЛжЧЕОВ¶ИЙэёЯЈ¬»ҜС§·ҙУҰЛЩВКФцҙуЈ¬NOөДЧӘ»ҜВКФцҙуЈ»ЖҪәвКұЈ¬NOөДЧӘ»ҜОӘ80%ЎЈјЩЙиНЁИлNOөДОпЦКөДБҝОӘxmolЈ¬АыУГИэөИКҪЈ¬УРЈә
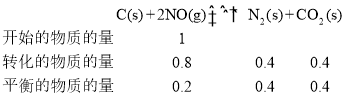
ФтCO2өДМе»э·ЦКэОӘ![]() Ј»
Ј»
ўЪИфNOөДЖрКјОпЦКөДБҝОӘ1molЈ¬јЩЙи·ҙУҰФЪәг¶ЁОВ¶ИәНұкЧјС№ЗҝПВҪшРРЈ¬NOөДЖҪәвЧӘ»ҜВКОӘҰБЈ¬ёщҫЭИэөИКҪЈ¬УРЈә
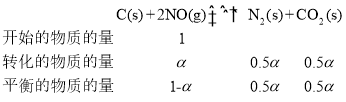
NOөДОпЦКөДБҝ·ЦКэОӘ![]() Ј¬Н¬АнN2әНCO2өДМе»э·ЦКэ·ЦұрОӘ0.5ҰБЎў0.5ҰБЈ»Фт
Ј¬Н¬АнN2әНCO2өДМе»э·ЦКэ·ЦұрОӘ0.5ҰБЎў0.5ҰБЈ»Фт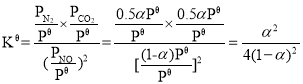 Ј»
Ј»
(4)ФЪХлНІЦРЈ¬Ме»эФҪРЎЈ¬С№ЗҝФҪҙуЈ¬ФцҙуС№ЗҝЈ¬ЖҪәвХэПтТЖ¶ҜЎЈ
ўЩМе»эФҪРЎЈ¬ёчОпЦКөДЕЁ¶ИФҪҙуЈ¬·ҙУҰЛЩВКФҪҙуЈ¬BөгөДС№ЗҝҙуЈ¬EөгөДС№ЗҝРЎЈ¬ДЗГҙBөгёчОпЦКөДЕЁ¶Иҙ󣬻ҜС§·ҙУҰЛЩВКҝмЈ¬ФтУРvB>vEЈ»
ўЪЖҪҫщПа¶Ф·ЦЧУЦКБҝ![]() Ј¬ёщҫЭЦКБҝКШәгЈ¬ЧЬЦКБҝmІ»ұдЈ¬ФтnФҪРЎЈ¬ЖҪҫщПа¶Ф·ЦЧУЦКБҝФҪҙуЎЈ·ҙУҰПтХэ·ҙУҰ·ҪПтҪшРРЈ¬n»бұдРЎЈ¬Фт·ҙУҰХэПтҪшРРөГФҪ¶аЈ¬ЖҪҫщПа¶Ф·ЦЧУЦКБҝФҪҙуЈ»EөгөҪFөгөД№эіМОӘС№ЛхМе»эөД№эіМЈ¬С№ЗҝЛІКұұдҙуЈ¬FөҪHОӘС№ЛхМе»эЈ¬ЖҪәвХэПтТЖ¶ҜөД№эіМЈ¬HҙпөҪЖҪәвЈ¬ФтHөгЈ¬ОпЦКөДЧЬОпЦКөДБҝnЧоРЎЈ¬ЖҪәвДҰ¶ыЦКБҝЧоҙуЎЈ
Ј¬ёщҫЭЦКБҝКШәгЈ¬ЧЬЦКБҝmІ»ұдЈ¬ФтnФҪРЎЈ¬ЖҪҫщПа¶Ф·ЦЧУЦКБҝФҪҙуЎЈ·ҙУҰПтХэ·ҙУҰ·ҪПтҪшРРЈ¬n»бұдРЎЈ¬Фт·ҙУҰХэПтҪшРРөГФҪ¶аЈ¬ЖҪҫщПа¶Ф·ЦЧУЦКБҝФҪҙуЈ»EөгөҪFөгөД№эіМОӘС№ЛхМе»эөД№эіМЈ¬С№ЗҝЛІКұұдҙуЈ¬FөҪHОӘС№ЛхМе»эЈ¬ЖҪәвХэПтТЖ¶ҜөД№эіМЈ¬HҙпөҪЖҪәвЈ¬ФтHөгЈ¬ОпЦКөДЧЬОпЦКөДБҝnЧоРЎЈ¬ЖҪәвДҰ¶ыЦКБҝЧоҙуЎЈ



| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝКөСйКТУГMnO2әНЕЁСОЛбЦЖИЎВИЖшКұЈ¬УР14.6 gВИ»ҜЗвұ»Сх»ҜЈ¬ЛщөГCl2И«ІҝУГКҜ»ТЛ®ОьКХЈ¬ҝЙЦЖөГЖҜ°Ч·ЫөДЦКБҝКЗ
A. 14.3 g B. 25.4 g C. 28.6 g D. 50.8 g
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ»ҜәПОпјЧ(![]() Ј¬
Ј¬![]() )Ј¬РФЦКАаЛЖВұЛШөҘЦКЎЈҪ«2.335gјЧјУИИЦБНкИ«·ЦҪвЈ¬ЙъіЙ0.01molТәМеТТәН224mL(ұкЧјЧҙҝцПВ)»ЖВМЙ«өДөҘЦКЖшМеұыЎЈЗл»ШҙрЈә
)Ј¬РФЦКАаЛЖВұЛШөҘЦКЎЈҪ«2.335gјЧјУИИЦБНкИ«·ЦҪвЈ¬ЙъіЙ0.01molТәМеТТәН224mL(ұкЧјЧҙҝцПВ)»ЖВМЙ«өДөҘЦКЖшМеұыЎЈЗл»ШҙрЈә
(1)јЧјУИИЦБНкИ«·ЦҪвөД»ҜС§·ҪіМКҪКЗ________ЎЈ
(2)ТТУлЛ®·ҙУҰөДАлЧУ·ҪіМКҪКЗ_________ЎЈ
(3)ПВБРУР№Ш»ҜәПОпјЧәНТТөДЛө·ЁХэИ·өДКЗ________ЎЈ(МоЧЦДё)
A.јЧІ»ДЬУлҝЙИјОпЎўјоАаТ»ЖрҙўФЛ
B.Т»¶ЁМхјюПВТТДЬУлТТП©»тұҪ·ҙУҰ
C.јЧ·ЦЧУЦРёчФӯЧУҫщҙпөҪ8өзЧУОИ¶ЁҪб№№
D.ҙЦөвЦРіЈ»мУРТТЈ¬ҝЙЦұҪУУГЙэ»Ә·Ё·ЦАлМбҙҝөв
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝЎ°М«СфЛ®ЎұөзіШЧ°ЦГИзНјЛщКҫЈ¬ёГөзіШУЙИэёцөзј«ЧйіЙЈ¬ЖдЦРaОӘTiO2өзј«Ј¬bОӘPtөзј«Ј¬cОӘWO3өзј«Ј¬өзҪвЦКИЬТәОӘpH=3өДLi2SO4-H2SO4ИЬТәЎЈп®АлЧУҪ»»»ДӨҪ«өзіШ·ЦОӘAЎўBБҪёцЗшЈ¬AЗшУлҙу ЖшПаНЁЈ¬BЗшОӘ·вұХМеПөІўУРN2ұЈ»ӨЎЈПВБР№ШУЪёГөзіШөДЛө·ЁҙнОуөДКЗЈЁ Ј©
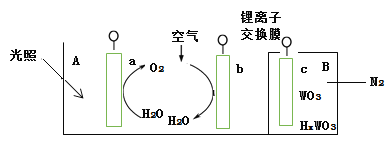
A.ИфУГөјПЯБ¬ҪУaЎўc,ФтaОӘёәј«Ј¬ёГөзј«ёҪҪьpHјхРЎ
B.ИфУГөјПЯБ¬ҪУaЎўc,Фтcөзј«өДөзј«·ҙУҰКҪОӘHxWO3 - xe- =WO3 + xH+
C.ИфУГөјПЯПИБ¬ҪУaЎўc,ФЩБ¬ҪУbЎўc,ҝЙКөПЦМ«СфДЬПтөзДЬЧӘ»Ҝ
D.ИфУГөјПЯБ¬ҪУbЎўc, bөзј«өДөзј«·ҙУҰКҪОӘO2+4H++4e-=2H2O
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝДіИЬТәЦРЦ»ә¬УРҙуБҝөДПВБРАлЧУЈәFe3+ЎўNO3ЎӘЎўK+әНMАлЧУЈ¬ҫӯІв¶ЁFe3+ЎўNO3ЎӘЎўK+әНMАлЧУөДОпЦКөДБҝЦ®ұИОӘ2:5:1:1Ј¬ФтMАлЧУҝЙДЬКЗ
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРРрКцХэИ·өДКЗЈЁ Ј©
A.ҪәМеөДұҫЦКМШХчКЗ¶Ўҙп¶ыР§УҰ
B.СжЙ«·ҙУҰКЗФӘЛШөДРФЦКЈ¬КфУЪ»ҜС§ұд»Ҝ
C.ГЬ¶ИОӘ1.84g/mlЎў98%өДБтЛбЈ¬ЖдОпЦКөДБҝЕЁ¶ИОӘ1.84mol/L
D.NAёцHCl·ЦЧУөДЦКБҝЈЁТФҝЛОӘөҘО»Ј©УлЖдПа¶Ф·ЦЧУЦКБҝФЪКэЦөЙППаөИ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝТТП©НӘЈЁCH2=C=OЈ©ФЪТ»¶ЁМхјюПВДЬёъә¬»оЖГЗвФӯЧУөД»ҜәПОп·ўЙъјУіЙ·ҙУҰЈ¬·ҙУҰөДНЁКҪҝЙұнКҫОӘCH2=C=O+HA=C=O+HAЎъ![]() (ј«І»ОИ¶Ё)Ўъ
(ј«І»ОИ¶Ё)Ўъ![]() КФЦёіцПВБР·ҙУҰІ»әПАнөДКЗЈЁЎЎ Ј©
КФЦёіцПВБР·ҙУҰІ»әПАнөДКЗЈЁЎЎ Ј©
A. CH2=C=O+HCl![]() CH3COCl
CH3COCl
B. CH2=C=O+H2O![]() CH3COOH
CH3COOH
C. CH2=C=O+CH3CH2OH![]() CH3COCH2CH2OH
CH3COCH2CH2OH
D. CH2=C=O+CH3COOH![]() ЈЁ CH3 C OЈ©2O
ЈЁ CH3 C OЈ©2O
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБР·ҪіМКҪКйРҙІ»ХэИ·өДКЗ( )
A. ТТП©К№деөДЛДВИ»ҜМјИЬТәНКЙ«Јә Br2+ CH2=CH2Ўъ CH2BrCH2Br
B. УГ¶иРФөзј«өзҪвВИ»ҜДЖИЬТәЈә 2Cl -+ 2H2O![]() H2+Cl2Ўь+ 2OH-
H2+Cl2Ўь+ 2OH-
C. КөСйКТЦЖТТИІЈә CaC2 + 2H2O Ўъ C2H2Ўь + Ca(OH)2
D. деТТЛбУлЗвСх»ҜДЖИЬТә№ІИИЈә BrCH2COOH+OH-![]() BrCH2COO-+H2O
BrCH2COO-+H2O
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝФЪўЩЎўўЪЎўўЫИЭ»эІ»өИөДәгИЭГЬұХИЭЖчЦРЈ¬ҫщідИл0.1molCOәН0.2molH2Ј¬ФЪҙЯ»ҜјБөДЧчУГПВ·ўЙъ·ҙУҰЈәCO(g)+2H2(g)![]() CH3OH(g)ЎЈІвөГИэёцИЭЖчЦРЖҪәв»мәПОпЦРCH3OHөДМе»э·ЦКэЛжОВ¶ИөДұд»ҜИзНјЛщКҫЈәПВБРЛө·ЁХэИ·өДКЗЈЁ Ј©
CH3OH(g)ЎЈІвөГИэёцИЭЖчЦРЖҪәв»мәПОпЦРCH3OHөДМе»э·ЦКэЛжОВ¶ИөДұд»ҜИзНјЛщКҫЈәПВБРЛө·ЁХэИ·өДКЗЈЁ Ј©
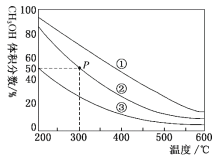
A.ёГ·ҙУҰөДХэ·ҙУҰОӘОьИИ·ҙУҰ
B.ИэёцИЭЖчИЭ»эЈәўЩ>ўЪ>ўЫ
C.ФЪPөгЈ¬COЧӘ»ҜВКОӘ75%
D.ФЪPөгЈ¬ПтИЭЖчўЪЦРФЩідИлCOЎўH2ј°CH3OHёч0.025molЈ¬ҙЛКұv(CO)Хэ>v(CO)Дж
Ійҝҙҙр°ёәНҪвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com