
| A. | 2AlCl3(熔融)$\frac{\underline{\;通电\;}}{\;}$ 2Al+3Cl2↑ | B. | 2NaCl(熔融)$\frac{\underline{\;通电\;}}{\;}$ 2Na+Cl2↑ | ||
| C. | Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | D. | 2HgO $\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑ |
分析 金属冶炼是工业上将金属从含有金属元素的矿石中还原出来的生产过程.金属的活动性不同,可以采用不同的冶炼方法.
金属冶炼的方法主要有:热分解法:对于不活泼金属,可以直接用加热分解的方法将金属从其化合物中还原出来(Hg及后边金属);
热还原法:在金属活动性顺序表中处于中间位置的金属,通常是用还原剂(C、CO、H2、活泼金属等)将金属从其化合物中还原出来(Zn~Cu);
电解法:活泼金属较难用还原剂还原,通常采用电解熔融的金属化合物的方法冶炼活泼金属(K~Al).
解答 解:A、氯化铝为共价化合物,在熔融状态不能电离出铝离子,不导电,所以不能用电解熔融氯化铝的方法制取铝,通常用电极氧化铝的方法制取铝,故A错误;
B、金属钠是活泼金属,工业上采用电解熔融物的方法冶炼,故B正确;
C、工业上采用热还原法来冶炼金属铁,故C正确;
D、对于不活泼金属Hg,可以直接用加热分解的方法将金属从氧化汞中还原出来,故D正确.
故选A.
点评 本题考查了金属冶炼的一般原理,难度不大,注意根据金属的活泼性不同采取相应的冶炼方法.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:多选题
| A. | 140℃时,无水乙醇与浓硫酸共热可制备乙烯 | |
| B. | 往油脂中加稀硫酸与之共热可发生皂化反应 | |
| C. | 可用碘溶液检验淀粉是否水解完全 | |
| D. | 验证溴乙烷中的溴元素,可直接加AgNO3溶液观察是否有淡黄色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L 0.1mol/L的氨水中有0.1NA个NH4+ | |
| B. | 标准状况下,22.4L盐酸含有NA个HCI分子 | |
| C. | 常温常压下,14g由N2与CO的混合气体含有0.5NA个原子 | |
| D. | 标准状况下,6.72L N02与水充分反应转移0.2NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,氧化产物是K2SO3,氧化剂与还原剂的物质的量之比为2:1,若反应中消耗了0.6molS,则反应中转移的电子为0.8mol.
,氧化产物是K2SO3,氧化剂与还原剂的物质的量之比为2:1,若反应中消耗了0.6molS,则反应中转移的电子为0.8mol.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
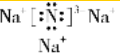 ,该化合物是由离子键形成的.
,该化合物是由离子键形成的.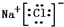 、
、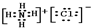 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸、纯碱、石膏、铁红 | B. | 醋酸、烧碱、纯碱、生石灰 | ||
| C. | 碳酸、熟石膏、小苏打、三氧化硫 | D. | 氯化氢、苛性钠、氯化钠、石灰石 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
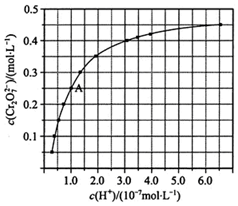 (1)CrO42-和Cr2O72-在溶液中可相互转化.室温下,初始浓度为1.0mol•L-1的Na2CrO4溶液中c(Cr2O72-)随c(H+)的变化如图所示.
(1)CrO42-和Cr2O72-在溶液中可相互转化.室温下,初始浓度为1.0mol•L-1的Na2CrO4溶液中c(Cr2O72-)随c(H+)的变化如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com