
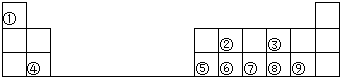
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
分析 由元素在周期表中位置,可知①为Na、②为K、③为Mg、④为Ca、⑤为Al、⑥为C、⑦为O、⑧为Cl、⑨为Br、⑩为Ar.
(1)稀有气体原子最外层为稳定结构,化学性质最不活泼;同周期自左而右原子半径减小、同主族自上而下原子半径增大;
(2)非金属性越强,最高价氧化物对应水化物的碱性越强;
(3)电子层结构相同的离子,核电荷数越大离子半径越小,离子的电子层越多离子半径越大;
(4)元素⑦的氢化物和元素钾单质反应,应是钾与水反应生成氢氧化钾与氢气;
(5)①⑨形成的化合物为NaBr,含有钠元素,焰色反应为黄色;溴化钠与氯气反应生成氯化钠与溴单质;
(6)Mg在二氧化碳中燃烧生成MgO与碳单质;溴的四氯化碳溶液为橙红色;非金属性越强,对应氢化物越稳定.
解答 解:由元素在周期表中位置,可知①为Na、②为K、③为Mg、④为Ca、⑤为Al、⑥为C、⑦为O、⑧为Cl、⑨为Br、⑩为Ar.
(1)稀有气体Ar原子最外层为稳定结构,化学性质最不活泼;同周期自左而右原子半径减小、同主族自上而下原子半径增大,故上述元素中K的原子半径最大,
故答案为:Ar;K;
(2)金属性K>Na>Al,非金属性越强,最高价氧化物对应水化物的碱性越强,故碱性:KOH>NaOH>Al(OH)3,
故答案为:KOH>NaOH>Al(OH)3;
(3)电子层结构相同的离子,核电荷数越大离子半径越小,离子的电子层越多离子半径越大,故离子半径:S2->K+>Ca2+>Na+>Mg2+>Al3+,
故答案为:S2->K+>Ca2+>Na+>Mg2+>Al3+;
(4)元素⑦的氢化物为H2O,钾与水反应生成氢氧化钾与氢气,化学反应方程式为:2K+2H2O=2KOH+H2↑,
故答案为:H2O;2K+2H2O=2KOH+H2↑;
(5)①⑨形成的化合物为NaBr,含有钠元素,该化合物灼烧时火焰焰色为黄色;溴化钠与氯气反应生成氯化钠与溴单质,化学反应方程式为:2NaBr+Cl2=2KCl+Br2,
故答案为:黄色;2NaBr+Cl2=2KCl+Br2;
(6)Mg在二氧化碳中燃烧生成MgO与碳单质,化学反应方程式为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,
⑥⑧形成化合物为四氯化碳,溴的四氯化碳溶液为橙红色,
由于非金属性Cl>Br,故氢化物稳定性HCl>HBr,
故答案为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;橙红色;HCl>HBr.
点评 本题考查元素周期表与元素周期律,关键是识记周期表中各元素,注意对元素化合物知识、元素周期律以及微粒半径大小比较的掌握.


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:选择题
| A. | HClO3 | B. | CaCl2 | C. | Cl2O7 | D. | Cl2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
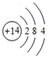 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从1L1mol/L的NaCl溶液中取出500 ml,其浓度是0.5mol/L | |
| B. | 制成0.5L10mol/L的盐酸,需要氯化氢气体112L(标准状况) | |
| C. | 0.5L 2mol/LBaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023 | |
| D. | 10g 98%硫酸(密度为1.84g/cm3)与1OmL 18.4mol/L硫酸的浓度是相同的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、Ag+、NO3-、SO42- | B. | Mg2+、NH4+、NO3-、Cl- | ||
| C. | Cu2+、Cl-、NO3-、Cl- | D. | K+、Na+、ClO-、S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S在过量的O2中充分燃烧,可得SO3 | |
| B. | 除去在Na2CO3固体中混有的NaHCO3的最好办法是通入过量的CO2 | |
| C. | 鉴别NaHCO3溶液与Na2CO3溶液,可用澄清的石灰水 | |
| D. | 等物质的量的Na2CO3和NaHCO3与盐酸反应,消耗HCl的物质的量之比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从食盐溶液中获得食盐晶体采用降温结晶的方法 | |
| B. | 除去酒精中含有的少量水采用蒸馏的方法 | |
| C. | 除去氯化钠溶液中少量的泥沙用蒸馏的方法 | |
| D. | 从碘水中获得碘的晶体采用过滤的方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5mol | B. | 0.1mol | C. | 2mol | D. | 1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{32a}{b}$ | B. | $\frac{32b}{a}$ | C. | $\frac{32b}{a}$mol-1 | D. | $\frac{32a}{b}$mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com