
分析 根据公式ρ=$\frac{m}{V}$进行判断;先分析每个分子中的质子数,再判断相同物质的量的三种分子含有的质子数;先分析每个分子中的电子数,再判断相同体积的三种物质中含有的电子数.
解答 解:(1)密度公式为:ρ=$\frac{m}{V}$=$\frac{M}{{V}_{m}}$,相同条件下,Vm相同,所以其密度之比等于其摩尔质量之比,为1:2:3,故答案为:1:2:3;
(2)每个H2、D2、T2分子中含有的质子数都是2,物质的量相同的三种单质含有的分子数相同,含有的质子数相同,所以为:1:1:1,故答案为:1:1:1;
(3)每个H2、D2、T2分子中含有的电子数都是2,相同条件下,体积相同的三种单质中含有的电子数相等,所以比为:1:1:1,故答案为:1:1:1.
点评 本题考查物质的量的有关计算原子结构等,比较基础,注意对基础知识的理解掌握,题目难度不大.


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 铝的密度小,熔点较低 | |
| B. | 铝在空气中燃烧,放出大量的热 | |
| C. | 铝在金属活动性顺序表排在较前面 | |
| D. | 铝具有还原性.发生氧化还原反应时放出大量的热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原电池的负极发生还原反应 | |
| B. | 电化学反应的实质是金属单质失去电子形成阳离子,而电子直接给氧化剂 | |
| C. | 金属在潮湿环境中主要发生析氢腐蚀 | |
| D. | 铜铁在潮湿的中性环境中锈蚀时,开始有Fe(OH)2,而后逐渐变成Fe(OH)3和Fe2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:M>Z>Y | |
| B. | Z元素的最高价氧化物的水化物的化学式为HZO4 | |
| C. | M2Y2中阴离子与阳离子的个数比为1:1 | |
| D. | X的氢化物的沸点低于Y的氢化物的沸点 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②④⑥ | C. | ①③⑥ | D. | ③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1NaOH溶液:K+、Na+、SO42-、CO32- | |
| B. | 能与铝反应放出氢气的溶液中:K+、SO42-、NO3-、NH4+ | |
| C. | 0.1 mol•L-1FeCl3溶液:K+、NH4+、I-、SCN- | |
| D. | c(H+)/c(OH-)=1×1014的溶液:Ca2+、Na+、ClO-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH值都为4的稀盐酸和NH4Cl溶液中,水的电离程度相同 | |
| B. | 浓度均为0.1mol/L的醋酸和NaOH溶液等体积混合后:lg[$\frac{c({H}^{+})}{c(O{H}^{-})}$]=0 | |
| C. | 在含浓度都为0.01mol/L的Cl-、CrO42-的混合溶液中滴加AgNO3溶液,先出现沉淀的是AgCl.[已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12] | |
| D. | 浓度均为0.1mol/L的NH4Cl和CH3COONH4溶液中,c(NH4+)相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
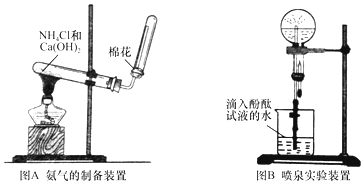
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com