
A”¢B”¢C”¢D”¢EĪŖĒ°36ŗÅŌŖĖŲ£¬ĖüĆĒµÄŗĖµēŗÉŹżŅĄ“ĪµŻŌö£¬ŅŃÖŖ£ŗAŹĒŌ×Ó°ė¾¶×īŠ”µÄŌŖĖŲ£»BŌ×ÓŗĖĶāÓŠĮ½øöĪ“³É¶Ōµē×Ó£¬ĒŅBŹĒŠĪ³É»ÆŗĻĪļÖÖĄą×ī¶ąµÄŌŖĖŲ£»B”¢C”¢D“¦ÓŚĶ¬ÖÜĘŚ£¬CµÄµŚŅ»µēĄėÄÜ“óÓŚĒ°ŗóĻąĮŚŌŖĖŲ£»DµÄµēøŗŠŌ½Ļ“󣬽ö“ĪÓŚ·śŌŖĖŲ£»EŹĒĒ°ĖÄÖÜĘŚÖŠĪ“³É¶Ōµē×ÓŹż×ī¶ąµÄŌŖĖŲ£®
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©EŌŖĖŲŌ×ÓµÄĶāĪ§µē×ÓÅŲ¼Ź½ĪŖ £¬CµÄµŚŅ»µēĄėÄÜ“óÓŚĘäŗóĆęĻąĮŚŌŖĖŲµÄŌŅņŹĒ £»
£Ø2£©ŹµŃé²āµĆA2DµÄÕōĘųĆܶȱČĻąĶ¬Ģõ¼žĻĀĄķĀŪÖµĆ÷ĻŌĘ«“󣬷ÖĪöæÉÄܵÄŌŅņŹĒ £®
£Ø3£©A”¢B”¢CŠĪ³ÉµÄČżŌ×Ó·Ö×ÓÖŠBµÄŌӻƹģµĄĄąŠĶĪŖ £¬øĆ·Ö×ÓÖŠŗ¬ÓŠµÄ¦Ņ¼üŗĶ¦Š¼üµÄŹżÄæÖ®±ČĪŖ £®
£Ø4£©+3¼ŪµÄEŠĪ³ÉµÄ°ĖĆęĢåÅäŗĻĪļECla•bNH3£¬Čō1molÅäŗĻĪļÓė×ćĮæAgNO3ČÜŅŗ×÷ÓĆÉś³É2molAgCl³Įµķ£¬Ōņb= £®

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗ£ÄĻ»ŖĒČ֊ѧȿŃĒѧŠ£ø߶žĻĀĘŚÄ©ĄķæĘ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÉčNAĪŖ°¢·üŁ¤µĀĀŽ³£Źż£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø £©
A£®28gC2H4Ėłŗ¬¹²ÓƵē×Ó¶ŌŹżÄæĪŖ4NA
B£®1L0.1mol•L©1ŅŅĖįČÜŅŗÖŠH+ŹżĪŖ0.1NA
C£®1mol¼×Ķé·Ö×ÓĖłŗ¬ÖŹ×ÓŹżĪŖ10NA
D£®±ź×¼×“æöĻĀ£¬22.4LŅŅ“¼µÄ·Ö×ÓŹżĪŖNA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÕć½Ź”ÉÜŠĖŹŠÖīōߏŠøß漶žÄ£»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ė«¼¶Ä¤µēÉųĪö½āĄėNaClČÜŅŗÖʱøĖį¼īµÄŌĄķ£¬ĪŖĢįøßŗ£Ė®µ»ÆµÄø½¼ÓÖµĢį¹©ĮĖŠĀµÄ¼¼ŹõĀ·¾¶£®ŅŃÖŖBPĪŖĖ«¼¶Ä¤£¬ŅõŃōĤ½ēĆęæÉŅŌ½āĄėH+ŗĶOH©£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
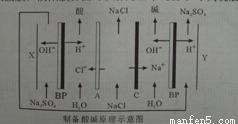
A£®AĪŖŃōĄė×Ó½»»»Ä¤£¬CĪŖŅõĄė×Ó½»»»Ä¤
B£®XĪŖŅõ¼«£¬·¢ÉśµÄµē¼«·“Ó¦·½³ĢŹ½ĪŖ£ŗ4OH©©4e©=O2”ü+2H2O
C£®ŌŚX”¢Y¼«ŹŅ¼ÓČėNa2SO4£¬ÄæµÄŹĒĢį¹©ÖʱøµÄĖįŗĶ¼īµÄŃōĄė×Ó»ņŅõĄė×Ó
D£®ĶعżøĆ×°ÖĆ£¬²»µ«ŗ£Ė®µĆµ½ĮĖµ»Æ£¬Ķ¬Ź±»¹æÉŅŌµĆµ½NaOH”¢HCl”¢H2”¢O2µČĪļÖŹ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģø£½ØŹ”ÄĻĘ½ŹŠĘÖ³ĒĻŲøßæ¼Ä£Äā»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ń”Ļī | Ļą¹ŲĖµ·Ø | Ö÷ŅŖŌŅņ |
A | °ü×°ÄŚ·ÅÖĆĶøĘųµÄ¹č½ŗ°ü£¬ÓŠĄūÓŚ·ĄÖ¹Ź³Ę·±äÖŹ | ¹č½ŗÓŠĒæĪüĖ®ŠŌ |
B | Ćę·Ū¼Ó¹¤³µ¼äŠü¹ŅÓŠ”°ŃĻ½ūŃĢ»š”±µÄÅĘ×Ó | ŃĢ»š»įĪŪČ¾Ćę·Ū |
C | ijŠ©ĢśÖĘĘ·³ö³§Ź±ŌŚĘä±ķĆęĶæÉĻŅ»²ćÓĶĤæÉ·ĄÖ¹ĘäÉśŠā | Ģś±»Ńõ»Æ£¬ŌŚĘä±ķĆęŠĪ³ÉŅ»²ćÖĀĆܵı£»¤Ä¤ |
D | ¾ŪĀČŅŅĻ©±”Ĥ²»ÄÜÓĆÓŚ°ü×°Ź³Ę· | »įŌģ³É°×É«ĪŪČ¾ |
A£®A B£®B C£®C D£®D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğÉĻŗ£ŹŠĒąĘÖĒųøß漶žÄ£»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ČēĶ¼ĖłŹ¾µÄ×°ÖĆÖŠ·¢Éś·“Ó¦2A2£Øg£©+B2£Øg£©?2C£Øg£©”÷H=©a kJ/mol£Øa£¾0£©£¬ŅŃÖŖPŹĒæÉ×ŌÓÉ»¬¶ÆµÄ»īČū£®ŌŚĻąĶ¬ĪĀ¶ČŹ±¹Ų±ÕK£¬ĻņČŻ»żĻąĶ¬µÄA”¢BČŻĘ÷ÖŠ·Ö±š¶¼³äČė2mol A2ŗĶ1mol B2ĘųĢ壮Į½ČŻĘ÷·Ö±šŌŚ500”ę“ļĘ½ŗāŹ±£¬AÖŠCµÄÅضČĪŖc1 mol/L£¬·Å³öČČĮæb kJ£¬BÖŠCµÄÅضČĪŖc2 mol/L£¬·Å³öČČĮæc kJ£®ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø £©

A£®500”ę“ļĘ½ŗāŹ±ÓŠ£ŗc1£¾c2
B£®500”ę“ļĘ½ŗāŹ±ÓŠ£ŗa£¾b£¾c
C£®“ļĘ½ŗāŗó“ņæŖK£¬ČŻĘ÷BµÄĢå»ż½«¼õŠ”
D£®“Ė·“Ó¦µÄĘ½ŗā³£ŹżĖęĪĀ¶ČÉżø߶ųŌö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğĮÉÄžŹ”ŗłĀ«µŗŹŠĮłŠ£Š×÷ĢåĮŖæ¼ø߶žĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ĻÖÓŠ²æ·Ö¶ĢÖÜĘŚŌŖĖŲµÄŠŌÖŹ»ņŌ×Ó½į¹¹ČēĻĀ±ķ£ŗ
ŌŖĖŲ | ŌŖĖŲŠŌÖŹ»ņŌ×ӵĽį¹¹ |
T | 2p¹ģµĄÄܼ¶µē×ÓŹż±ČsÄܼ¶µē×ÓŹż¶ą1øö |
X | L²ćpÄܼ¶µē×ÓŹż±ČsÄܼ¶µē×ÓŹż¶ą2øö |
Y | µŚČżÖÜĘŚŌŖĖŲµÄ¼ņµ„Ąė×ÓÖŠ°ė¾¶×īŠ” |
Z | L²ćÓŠ3øöĪ“³É¶Ōµē×Ó |
£Ø1£©Š“³öŌŖĖŲXµÄĄė×Ó½į¹¹Ź¾ŅāĶ¼£ŗ £®Š“³öŌŖĖŲZµÄ¼ņµ„ĘųĢ¬Ēā»ÆĪļµÄµē×ÓŹ½£ŗ £®
£Ø2£©Š“³öŌŖĖŲYµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļÓėKOH·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ £®
£Ø3£©T”¢Y”¢ZČżÖÖŌŖĖŲµÄµ„ÖŹÖŠ»ÆѧŠŌÖŹĆ÷ĻŌ²»Ķ¬ÓŚĘäĖūµ„ÖŹµÄŹĒ £ØĢīŌŖĖŲ·ūŗÅ£¬ĻĀĶ¬£©£»ŌŖĖŲTÓėĀČ»ÆĖŲĻą±Č£¬·Ē½šŹōŠŌ½ĻĒæµÄŹĒ £¬ĻĀĮŠ±ķŹöÖŠÄÜÖ¤Ć÷ÕāŅ»ŹĀŹµµÄŹĒ £ØĢī×ÖÄø£©£®
a£®³£ĪĀĻĀĀČĘųµÄŃÕÉ«±ČTµ„ÖŹµÄŃÕÉ«Éī
b£®TµÄµ„ÖŹĶØČėĀČ»ÆÄĘĖ®ČÜŅŗÖŠ²»ÄÜÖĆ»»³öĄ“
c£®ĀČÓėTŠĪ³É»ÆŗĻĪļÖŠ£¬ĀČŌŖĖŲ³ŹÕż¼Ū£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğĮÉÄžŹ”ŗłĀ«µŗŹŠĮłŠ£Š×÷ĢåĮŖæ¼ø߶žĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĪļÖŹ²»ŹōÓŚÅäŗĻĪļµÄŹĒ£Ø £©
A£®K3[Fe£ØCN£©6]
B£®MgCl2
C£®[Cu£ØH2O£©4]SO4•H2O
D£®[Ag£ØNH3£©2]OH
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ½ĖÕŹ”ÄĻĶØŹŠČēøŽŹŠøßŅ»ĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
½«7.8gĆ¾ĀĮŗĻ½š¼ÓČė100mL 5.0mol•L©1NaOHČÜŅŗÖŠ£¬³ä·Ö·“Ó¦ŗóŹÕ¼Æµ½6.72LĘųĢå£Ø±ź×¼×“æö£©£¬¹żĀĖµĆµ½ČÜŅŗX£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®²śÉśĘųĢåµÄÖŹĮæĪŖ0.3g
B£®ŗĻ½šÖŠĆ¾ÓėĀĮµÄĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ2
C£®ČÜŅŗXÖŠŹ£ÓąNaOHµÄĪļÖŹµÄĮæĪŖ0.2 mol
D£®ĻņČÜŅŗXÖŠĶØČė×ćĮæC02£¬¹żĀĖ£¬½«³Įµķ³ä·Ö×ĘÉÕµĆ¹ĢĢå15.6 g
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016Ń§ÄźÉ½¶«Ź”ø߶žĻĀ6ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
¹¤ŅµÉĻÓŠŅ»ÖÖ·½·ØÓŠŠ§µŲæŖ·¢ĄūÓĆCO2£¬ŹĒÓĆCO2Ą“Éś²śČ¼ĮĻ¼×“¼”£ĪŖĢ½¾æ·“Ó¦ŌĄķ£¬½ųŠŠČēĻĀŹµŃ飬ŌŚĢå»żĪŖ1LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ£¬³äČė1molCO2ŗĶ3molH2£¬Ņ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦£ŗCO2£Øg£©+3H2£Øg£© CH3OH£Øg£©+H2O£Øg£©£»”÷H=-49.0kJ/mol£®²āµĆCO2ŗĶCH3OH£Øg£©µÄÅضČĖꏱ¼ä±ä»ÆČēĶ¼ĖłŹ¾”£
CH3OH£Øg£©+H2O£Øg£©£»”÷H=-49.0kJ/mol£®²āµĆCO2ŗĶCH3OH£Øg£©µÄÅضČĖꏱ¼ä±ä»ÆČēĶ¼ĖłŹ¾”£

£Ø1£©“Ó·“Ó¦æŖŹ¼µ½Ę½ŗā£¬ĒāĘųµÄĘ½¾ł·“Ó¦ĖŁĀŹv£ØCO2£©= ________mol/£ØL•min£©£»
£Ø2£©ĒāĘųµÄ×Ŗ»ÆĀŹ= ________£»
£Ø3£©Ēó“ĖĪĀ¶ČĻĀøĆ·“Ó¦µÄĘ½ŗā³£ŹżK=________£»
£Ø4£©ĻĀĮŠ“ėŹ©ÖŠÄÜŹ¹Ę½ŗāĢåĻµÖŠn£ØCH3OH£©/n£ØCO2£©Ōö“óµÄŹĒ________
A£®½«H2O£Øg£©“ÓĢåĻµÖŠ·ÖĄė³öČ„
B£®³äČėHe£Øg£©£¬Ź¹ĢåĻµŃ¹ĒæŌö“ó
C£®ÉżøßĪĀ¶Č
D£®ŌŁ³äČė1mol CO2ŗĶ3mol H2
£Ø5£©µ±·“Ó¦“ļµ½Ę½ŗāŹ±£¬CO2µÄĪļÖŹµÄĮæÅضČĪŖc1£¬Č»ŗóĻņČŻĘ÷ÖŠŌŁ¼ÓČėŅ»¶ØĮæCO2£¬“ż·“Ó¦ŌŁŅ»“Ī“ļµ½Ę½ŗāŗó£¬CO2µÄĪļÖŹµÄĮæÅضČĪŖc2£¬Ōņc1________ c2£ØĢī£¾”¢£¼”¢£½£©
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com