
【题目】硫在空气中燃烧可以生成SO2,SO2在催化剂作用下可以被氧化为SO3,其热化学方程式可表示为:S(g) +O2(g)═SO2(g) △H=-297kJ/mol,SO2(g) + 1/2O2(g)![]() SO3(g);△H =-98.3 KJ/mol。下图是上述两个反应过程与能量变化的关系图,其中Ⅰ表示0.4mol SO2(g)、1.6molSO3(g)、0.2mol O2(g)具有的能量,Ⅲ表示64gS(g)与96g O2(g)所具有的能量。
SO3(g);△H =-98.3 KJ/mol。下图是上述两个反应过程与能量变化的关系图,其中Ⅰ表示0.4mol SO2(g)、1.6molSO3(g)、0.2mol O2(g)具有的能量,Ⅲ表示64gS(g)与96g O2(g)所具有的能量。
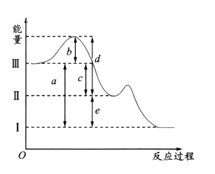
(1)Ⅰ→Ⅱ的反应是________(填“吸热”,“放热”)反应。
(2)c为____________KJ。
(3)图示中b的大小对Ⅲ→Ⅱ反应的△H的影响是______。
A.△H随着b的增大而增大
B.△H随着b的增大而减小
C.△H随着b的减小而增大
D.△H不随b的变化而变化
(4)上图中的d+e-b=________________KJ。
【答案】 吸热 594 D 751.28
【解析】试题分析:
(1)从图像可知,Ⅱ的能量比Ⅰ高,则Ⅰ→Ⅱ的反应是吸热反应。
(2)从图像可知,c为64gS(g)与96g O2(g)完全反应后的热效应,因O2过量,则按照S的物质的量计算,根据S(g) +O2(g)═SO2(g) △H=-297kJ/mol,则64gS(g),即2molS(g)完全反应放出的热量c为297×2=594KJ。
(3)化学反应的反应热与活化能无关,则△H不随b的变化而变化,故选D。
(4)上图中的d+e-b为64gS(g)与96g O2(g)最终反应生成0.4mol SO2(g)、1.6molSO3(g)、0.2mol O2(g)所释放的能量,则64gS(g)与96g O2(g)反应生成2mol SO2(g)时放出594KJ的热量,然后2mol SO2(g)、1mol O2(g)反应生成0.4mol SO2(g)、1.6molSO3(g)、0.2mol O2(g)时共消耗了1.6mol SO2(g),根据SO2(g) + 1/2O2(g)![]() SO3(g);△H ="-98.3" KJ/mol可知,放出热量为98.3 KJ/mol×1.6mol="157.28" KJ。所以共放出热量为594KJ+157.28 KJ="751.28" KJ。即上图中的d+e-b="751.28" KJ。
SO3(g);△H ="-98.3" KJ/mol可知,放出热量为98.3 KJ/mol×1.6mol="157.28" KJ。所以共放出热量为594KJ+157.28 KJ="751.28" KJ。即上图中的d+e-b="751.28" KJ。


 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:
【题目】下列实验操作都要用玻璃棒:①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体,其中玻璃棒作用相同的是( )
A. ①和② B. ①和③ C. ①和④ D. ③和④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z均为短周期主族元素,且原子序数依次增大。已知W元素的原子形成的离子是一个质子;X、Y在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;Z为同周期中原子半径最大的元素。下列有关说法正确的是
A. 四种元素均为非金属元素
B. W与X、Y形成的最简单分子的沸点:X>Y
C. Y、Z形成的化合物中只含离子键
D. W、Y、Z形成的化合物的电子式为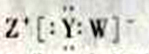
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验对应的现象及结论均正确,且两者具有因果关系的是
选项 | 实验 | 现象 | 结论 |
A | 向稀硝酸与过量铜粉反应后的溶液中滴加稀硫酸 | 有气泡生成 | 常温下,铜与稀硫酸反应生成SO2 |
B | 在酒精灯上加热铝箔 | 铝熔化,但熔化的铝不滴落 | Al2O3的熔点比Al高 |
C | 向Fe(SCN)3溶液中滴加稀NaOH溶液 | 溶液有红色变为红褐色 | 减小反应物浓度、平衡向逆反应方向移动 |
D | 选用酚酞作试剂,用NaOH溶液滴定醋酸溶液 | 溶液变为粉红色 | NaOH溶液过量 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下、一定体积条件下,能说明下列反应达到平衡状态的是
A.反应2SO2(g)+O2(g)![]() 2SO3(g) 容器内的密度不随时间变化
2SO3(g) 容器内的密度不随时间变化
B.反应A2(g)+B2(g)![]() 2AB(g)容器内A2的消耗速率与AB消耗速率相等
2AB(g)容器内A2的消耗速率与AB消耗速率相等
C.反应N2+3H2![]() 2NH3容器内气体平均相对分子质量不随时间变化
2NH3容器内气体平均相对分子质量不随时间变化
D.反应4A(s)+3B(g)![]() 2C(g)+D(g)容器内气体总压强不随时间变化
2C(g)+D(g)容器内气体总压强不随时间变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定质量的Na、K分别投入足量的同浓度、同体积的稀盐酸中,在相同条件下产生氢气的体积随时间变化的曲线如图中a、b所示,则下列说法中不正确的是

A. 曲线a对应的反应使用了催化剂
B. 投入的Na、K物质的量相等
C. 曲线a代表K的反应,曲线b代表Na的反应
D. 两反应中反应速率不同的主要原因是反应物自身的性质不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应H2(g)+Cl2(g)═2HCl(g) 的发生过程能量变化如下所示:
![]()
下列说法错误的是
A.H﹣H键比Cl﹣Cl键稳定
B.△H=﹣184.5 kJmol﹣1
C.正反应活化能比逆反应活化能高
D.在相同条件下,1mol H2(g)和1mol Cl2(g)分别在点燃和光照条件下反应生成2mol HCl(g),重新恢复到原来的状态时△H相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱性硼化钒(VB2)-空气电池工作时反应为:4VB2+11O2=4B2O3+2V2O5。用该电池为电源,选用惰性电极电解硫酸铜溶液,当外电路中通过0.04 mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是
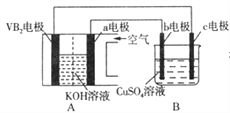
A. VB2电极发生的电极反应为:2VB2+11H2O-22e-=V2O5+2B2O3+22H+
B. 外电路中电子由c电极流向VB2电极
C. 电解过程中,b电极表面先有红色物质析出,然后有气泡产生
D. 若B装置内的液体体积为100mL,则CuSO4溶液的物质的量浓度为0.2mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com