
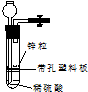
 有一兴趣小组准备在实验室中制H2,装置如图所示.可是在实验室中发现酸液不足而又无其他酸液可加入.为达到实验目的,可以从长颈漏斗中加入适量的试剂是( )
有一兴趣小组准备在实验室中制H2,装置如图所示.可是在实验室中发现酸液不足而又无其他酸液可加入.为达到实验目的,可以从长颈漏斗中加入适量的试剂是( )| A. | ①②③ | B. | ②④⑤ | C. | ①②④⑥ | D. | ②③⑥ |
分析 在实验室中发现酸液不足而又无其他酸液可加入实现制取氢气,则加入试剂为水溶液或与酸不反应不互溶且密度比水大的有机溶剂,以此来解答.
解答 解:①NaNO3溶液在酸性条件下与Zn反应不生成氢气,故错误;
②酒精可使液体总体积变大,Zn与稀硫酸接触而制取氢气,故正确;
③CCl4与硫酸不反应且密度比硫酸密度大,Zn与稀硫酸接触而制取氢气,故正确;
④苯的密度比硫酸密度小,隔绝Zn与稀硫酸,不能制备氢气,故错误;
⑤Na2CO3溶液与硫酸反应生成二氧化碳,不利于制备氢气,故错误;
⑥KCl溶液可使液体总体积变大,Zn与稀硫酸接触而制取氢气,故正确;
故选D.
点评 本题考查实验装置综合应用及物质的性质,为高频考点,把握制备氢气的反应原理、物质的性质为解答的关键,侧重分析与应用能力的考查,注意硝酸钠为解答的难点,题目难度不大.


科目:高中化学 来源: 题型:解答题
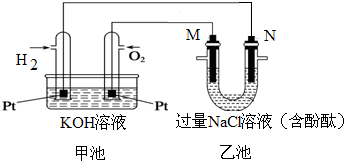 如图所示是氢氧燃料电池工作时的装置,乙池中的两个电极均是石墨电极,请回答下列问题:
如图所示是氢氧燃料电池工作时的装置,乙池中的两个电极均是石墨电极,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
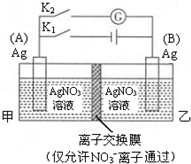
| A. | 闭合K1,断开K2后,A电极增重 | |
| B. | 闭合K1,断开K2后,乙池溶液中Ag+浓度增大 | |
| C. | 断开K1,闭合K2后,B电极发生氧化反应 | |
| D. | 断开K1,闭合K2后,NO3-向A电极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
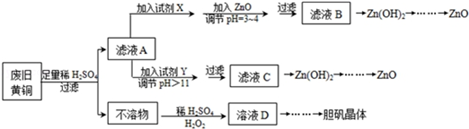
| Fe3+ | Fe2+ | Zn2+ | |
| 开始沉淀的pH | 1.1 | 5.8 | 5.9 |
| s沉淀完全的pH | 3.0 | 8.8 | 8.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na与氧气 | B. | 澄清石灰水与二氧化碳 | ||
| C. | Al与稀盐酸 | D. | KHCO3与Ba(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电器起火,立即用水扑灭 | |
| B. | 炒菜时油锅着火,立即盖上锅盖 | |
| C. | 厨房煤气管道漏气,立即关闭阀门并开窗通风 | |
| D. | 图书管内图书着火,立即用液态二氧化碳灭火器扑灭 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
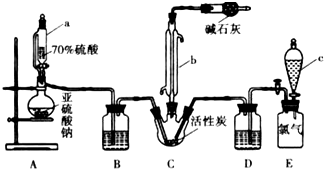 硫酰氯(SO2Cl2)是一种重要的化工试剂,实验室合成硫酰氯的实验装置如图所示:
硫酰氯(SO2Cl2)是一种重要的化工试剂,实验室合成硫酰氯的实验装置如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com