
已知:25℃时,电离常数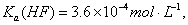 ,溶度积常数
,溶度积常数
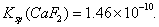 现向110.2 mol·L-1HF溶液中加入1L0.2 mo·L-l CaCl2溶液,则下列说法中正确的是 ( )
现向110.2 mol·L-1HF溶液中加入1L0.2 mo·L-l CaCl2溶液,则下列说法中正确的是 ( )
A.25℃时,0.1 mol.L-l HF溶液的pH=l
B. 随温度和浓度的变化而变化
随温度和浓度的变化而变化
C.该体系中有CaF2沉淀产生
D.升高温度, 将变小
将变小
科目:高中化学 来源: 题型:
为了讲授“氯气的性质和用途”,李老师以二氧化锰和浓盐酸为主要原料制取氯气,并设计了如图所示装置(其中A是连有注射器针头的橡皮管,针头已插入并穿过橡皮塞)进行教学.

试回答下列问题:
(1)乙中的现象是____________________ 丙中的现象是______________
甲的作用是 ____________________ 己的作用是____________
(2)写出己中反应的离子方程式:
________________________________________________________________.
(3)写出漂白液在生活中消毒杀菌的离子方程式:
________________________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
Na2O、NaOH、Na2 CO3、NaCl、Na2SO4可按某种标准划为同一类物质,下列分类标准正确的
CO3、NaCl、Na2SO4可按某种标准划为同一类物质,下列分类标准正确的
是 ( )
①钠的化合物 ②能与硝酸反应的物质 ③可溶于水的物质
④电解质 ⑤钠盐 ⑥钠的含氧化合物
A.①③④⑤ B.①②⑤⑥ C.①③④ D.②⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于反应能量的说法正确的是 ( )
A.Zn(s)+CuSO4 (aq)==ZnSO4 (aq) +Cu(s);△H=—216kJ·mol-1。则反应物总能量>生成物总能量
B.若一定条件下,A==B AH<O;说明A物质比B物质稳定
C.101kPa时,2H2(g)+O2(g)==2H2O(l);△H=—571.6kJ·mol-1,则H2的燃烧热为571. 6kJ·mol-l
D.H+(aq) +OH- (aq)=H2O(l);△H=-57. 3kJ.mol-1,含1mol NaOH的氢氧化钠溶液与含0. 5mol H2SO4的浓硫酸混合后放出57. 3kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性。

(1)D装置中电解饱和食盐水的离子反应方程式为:
(2)为检验氯气的氧化性,则E装置的溶液可以是 。
A.淀粉碘化钾溶液 B.酸性KMnO4溶液
C.FeCl2溶液 D.Na2S溶液
(3)F装置的目的是 。
(4)为测定Cu的相对原子质量,某同学设计了如下的方案:
精确测量硬质玻璃管的质量为a g,放入CuO后,精确测量硬质玻璃管和CuO的总质量为b g,实验完毕后(通过足量的氢气),通过精确测量硬质玻璃管和Cu粉的总质量为c g,进而确定Cu的相对原子质量。
①对B装置中的氧化铜粉末加热前,需要进行的操作为 ;
②A装置中盛放的试剂为 ;
③根据测得结果进行计算,则Cu的相对原子质量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是
A.K3C60在熔融状态下能够导电,所以K3C60是电解质
B.胶体和溶液的本质区别在于能否发生丁达尔现象
C.离子键的本质就是阴阳离子之间的相互吸引
D.变化过程中化学键被破坏,则一定发生化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
乙酸乙酯、甲酸甲酯、乙酸丙酯三种物质组成的混合酯中,若氧元素的质量分数为30%,那么氢元素的质量分数可能是( )
A、10% B、20% C、30% D、40%
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.溶液是电中性的,胶体是带电的
B.依据丁达尔效应可区分透明胶体和溶液
C.将4.0g NaOH溶于100g蒸馏水中,所得溶液物质的量浓度为1.0mol·L-1
D.CO2与SiO2都属于酸性氧化物,都能与水反应生成相应的酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com